
| A. | 25g质量分数68%的H2O2水溶液中含氧原子数目为NA | |
| B. | 0.1mol•L-1 NH4Cl溶液中含有NH4+的数目小于0.1NA | |
| C. | 100mL 12mol•L-1 的浓HNO3与过量Cu反应转移电子的数目为0.6NA | |
| D. | 标准状况下,11.2L由C2H4和C3H4 组成的混合气体中含有氢原子的数目为2NA |
分析 A.水分子、双氧水分子都含有氧原子;
B.溶液体积未知,无法计算;
C.浓HNO3与铜反应被还原为NO2,稀HNO3与铜反应被还原为NO;
D.根据CH4和C2H4均含4个氢原子来分析.
解答 解:A.双氧水和都含有氧原子,25g质量分数68%的H2O2水溶液中含氧原子数目大于NA,故A错误;
B.溶液体积未知,无法计算氨根离子的个数,故B错误;
C.由于浓HNO3与铜反应被还原为NO2,而稀HNO3与铜反应被还原为NO,100 mL 12 mol•L-1的浓HNO3中被还原为NO2和NO的物质的量不明确,故转移的电子数无法计算,故C错误;
D.标况下,11.2L混合气体的物质的量为0.5mol,而CH4和C2H4均含4个氢原子,故0.5mol混合气体中含有的氢原子的个数2NA,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,题目难度不大.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 任何纯净物都是由一种元素组成的 | |
| B. | 一种元素只能组成一种单质 | |
| C. | 任何一种化合物都是由不同种元素组成的 | |
| D. | 任何物质都是由分子构成的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子最外层只有两个电子的元素都在第ⅡA族 | |
| B. | 人们通常在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| C. | 共价化合物中可能含有离子键 | |
| D. | 水溶液能导电的化合物都是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
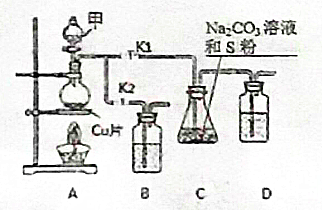 硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图1.
硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
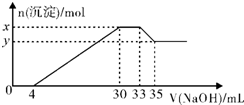 在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列叙述不正确的是( )
在200mL含Mg2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入5mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列叙述不正确的是( )| A. | 原溶液中n(Mg2+):n(Al3+)=5:1 | B. | 原溶液的c(H+)=0.1mol•L-1 | ||
| C. | x与y的差值为0.01mol | D. | 原溶液中c(Cl-)=0.85mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羟基的电子式 | B. | 醛基官能团符号-COH | ||
| C. | 乙醇的分子式:CH3CH2OH | D. | 异丁烷的结构简式:CH3CH(CH3)CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在元素周期表左下方区域的金属元素中寻找半导体材料 | |
| B. | 利用元素周期表中氟、氯、硫、磷附近的元素研制新型农药 | |
| C. | 在过渡金属中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| D. | 在周期表一定区域内寻找元素、发现物质的新用途是一种相当有效的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com