
| A. | 硅酸钠溶液 | B. | 氢氟酸 | C. | 蔗糖溶液 | D. | 氯化钠溶液 |
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:解答题
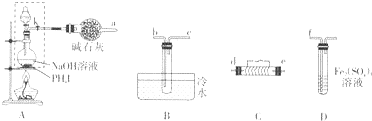
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用CCl4可擦去圆珠笔油渍 | |
| B. | 蚊虫叮咬处涂抹肥皂水可止痛痒 | |
| C. | 煮鱼时加入少量食醋和料酒可除腥味,增加香味 | |
| D. | 小苏打可用作焙制面包 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
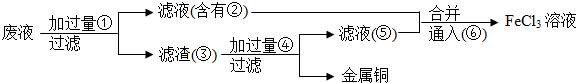
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
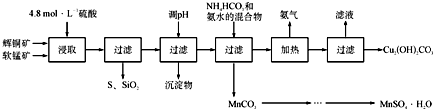
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Mn 2+ | 8.3 | 9.8 |
| Cu 2+ | 4.4 | 6.4 |
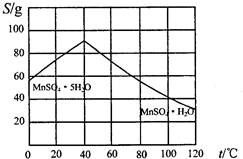
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将适量的发酵粉放在容器中加热,观察气体的产生 | |
| B. | 在洁净的水杯中先加入小苏打粉,再加入食醋,观察气体 | |
| C. | 往稀白粥中加入少量加碘食盐,检验加碘食盐中含有I2 | |
| D. | 在一瓣橘子上插入两根铜丝并与小灯泡连接,验证电流的产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验要求 | 化学试剂或实验方法 |
| 检验HCl中是否含Cl2 | |
| 从海水中获取淡水 | |
| 将Br2从水中分离出来 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com