
分析 (1)一般含C元素的一类化合物为有机物;
(2)物质导电的条件:存在自由电子或者自由移动的离子;在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
(3)金属与酸反应生成氢气;
(4)葡萄糖含-CHO,能与氢氧化铜反应生成砖红色沉淀氧化亚铜;
(5)能与⑥反应设计成电池为燃料电池,可燃性物质均符合.
解答 解:①甲烷为最简单的有机物,为化合物,为非电解质;
②NaCl晶体中离子不能自由移动,不导电,为电解质;
③金属镁为单质,含自由电子可导电;
④纯碱溶液为混合物,含自由离子,可导电;
⑤KOH溶液为混合物,含自由离子,可导电;
⑥O2为单质,不能导电;
⑦硫酸铜粉末中离子不能自由移动,不导电,为电解质;
⑧冰醋酸为化合物,由分子构成不导电,在水中可电离,为电解质;
⑨NaOH晶体中离子不能自由移动,不导电,为电解质;
⑩葡萄糖为有机物,具有还原性,为非电解质,
(1)以上物质中属于有机化合物的是①⑩,故答案为:①⑩;
(2)以上物质中能导电的物质是③④⑤,属于电解质的是②⑦⑧⑨,其中属于碱的电解质的电离方程式为NaOH=Na++OH-,
故答案为:③④⑤;②⑦⑧⑨;NaOH=Na++OH-;
(3)以上物质中能发生反应生成H2的离子方程式为Mg+2CH3COOH=Mg(CH3COO)2+H2↑,
故答案为:Mg+2CH3COOH=Mg(CH3COO)2+H2↑;
(4)在加热的条件下能与新制Cu(OH)2发生氧化还原反应的是⑩,还原产物的化学式为Cu2O,故答案为:⑩;Cu2O;
(5)以上物质中①、⑩均能燃烧,则一定条件下,能与⑥反应设计成电池,故答案为:①或⑩.
点评 本题考查氧化还原反应及物质分类等,综合性较强,注重基础知识的考查,把握相关概念及氧化还原反应为解答的关键,题目难度不大.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯水几乎不导电,因此水是非电解质 | |
| B. | 在任何温度下,纯水的pH均等于7 | |
| C. | 向水中加入钠,溶液中$\frac{{K}_{w}}{c(O{H}^{-})}$减小 | |
| D. | 向水中加入醋酸,c(H+)和水的电离均增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ.某学习小组用乙醇与氢溴酸为原料制备溴乙烷.
Ⅰ.某学习小组用乙醇与氢溴酸为原料制备溴乙烷.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
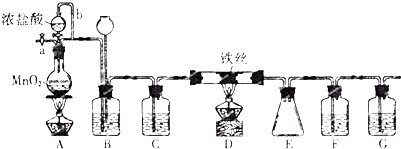
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
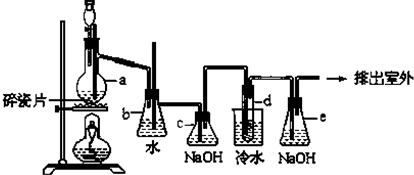
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| c(SO2)/mol•L-1 | 1.00 | 0.50 | 0.23 | 3.00×10-37 | 3.00×10-37 |
| c(CO)/mol•L-1 | 4.00 | 3.00 | 2.46 | 2.00 | 2.00 |
| A. | 当v(SO2)正=2v(CO)逆时,该反应达到了平衡状态 | |
| B. | X的化学式为CO2 | |
| C. | 前1s内v(X)=1.00mol•L-1•s-1 | |
| D. | 上述反应达到平衡时,CO的转化率为50% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com