


科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
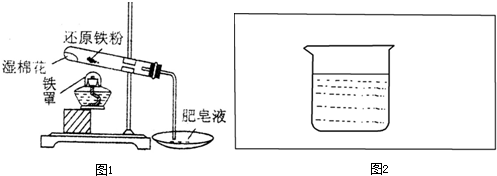
 ”表示),设计一套原电池装置,并验证有电流产生,请帮他在图2方框内补充全装置简图(要求标注正、负极及其材料和电解质溶液名称).
”表示),设计一套原电池装置,并验证有电流产生,请帮他在图2方框内补充全装置简图(要求标注正、负极及其材料和电解质溶液名称).查看答案和解析>>
科目:高中化学 来源: 题型:
请回答下列问题:
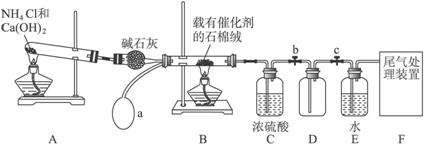
(1)写出装置A中主要反应的化学方程式______________________________________。
(2)已知1 mol NO2与液态水反应生成HNO3溶液和NO气体放出热量46 kJ,写出该反应的热化学方程式_______________________________________________________________。
该反应是一个可逆反应,欲提高NO2的转化率,可采取的措施是___________________。
A.降低温度 B.升高温度
C.减小压强 D.增大压强
(3)实验结束后,关闭止水夹b、c,将装置D浸入冰水中,现象是___________________。
(4)装置C中浓H2SO4的作用是_____________________________________________。
(5)请你帮助该化学小组设计实验室制取NH3的另一方案____________________________。
(6)干燥管中的碱石灰用于干燥NH3,某同学思考是否可用无水氯化钙代替碱石灰,并设计下图所示装置(仪器固定装置省略未画)进行验证。实验步骤如下:
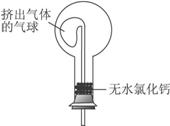
①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞。
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可观察到的现象是__________________,由此,该同学得出结论:不能用CaCl2代替碱石灰。
查看答案和解析>>
科目:高中化学 来源:模拟题 题型:实验题
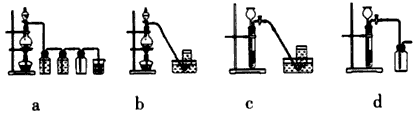
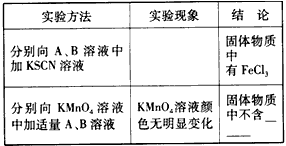

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
(1)对于可逆反应mA(g)+nB(g) ![]() pC(g)+qD(g)达平衡时,V正=k1c(A)mc(B)n(K1为速率常数),达平衡时化学平衡常数为K2,且K1、K2只与温度有关。现将4molSO2与2molO2充入体积为2L的密闭容器中,500℃进行反应并保持温度不变,反应达到平衡时,SO2的转化率为50%。则起始时正反应速率是平衡时的 倍。500℃时,该反应的平衡常数K2是 。在温度不变时,再向平衡体系中加人2molSO2、2molO2与4molSO3,平衡将向 移动。
pC(g)+qD(g)达平衡时,V正=k1c(A)mc(B)n(K1为速率常数),达平衡时化学平衡常数为K2,且K1、K2只与温度有关。现将4molSO2与2molO2充入体积为2L的密闭容器中,500℃进行反应并保持温度不变,反应达到平衡时,SO2的转化率为50%。则起始时正反应速率是平衡时的 倍。500℃时,该反应的平衡常数K2是 。在温度不变时,再向平衡体系中加人2molSO2、2molO2与4molSO3,平衡将向 移动。
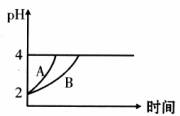
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如下图所示。则图中表示醋酸溶液中pH变化曲线的是 (填“A”或“B”)。
设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1 m2(选填“<”、“=”,“>”)。
(3)难溶电解质在水溶液中存在着电离平衡。在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(KSP)。当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。已知常温下Cu(OH)2的溶度积为2×10![]() ,若某CuSO4溶液里,c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于 ;要使0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为 。
,若某CuSO4溶液里,c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于 ;要使0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为 。
(4)常温下,某纯碱(Na2CO4)溶液中滴入酚酞,溶液呈红色。则该溶液呈 性。在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所至;乙同学认为是溶液中Na2CO3电离出的CO![]() 水解所至。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) 。
水解所至。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com