
【题目】根据化学方程式:(1)2Fe3++2I-=2Fe2++I2;(2)Br2+2Fe2+=2Br-+2Fe3+,可判断离子的还原性从强到弱的顺序是( )
A. Br-、Fe2+、I- B. I-、Fe2+、Br-
C. Br2、Fe3+、I2 D. Br-、I-、Fe2+
科目:高中化学 来源: 题型:
【题目】有关锌-稀硫酸-铜构成的原电池的一些说法中,正确的是( )
A. 锌片为正极,且锌片逐渐溶解
B. 铜片为负极,且铜片上有气泡
C. 溶液中的H+移向铜极
D. 该电池工作的过程中溶液的酸性始终不变
【答案】C
【解析】A、较活泼的金属锌作负极,选项A错误;B、较活泼的金属锌作负极,较不活泼的金属铜作正极,正极上氢离子得电子生成氢气,所以铜片上有气泡生成,选项B错误;C、原电池中阳离子H+移向正极铜电极,选项C正确;D、负极上锌失电子生成锌离子进入溶液,正极上氢离子得电子生成氢气析出,所以一段时间后溶液中H+浓度降低,酸性减弱,选项D错误。答案选C。
【题型】单选题
【结束】
25
【题目】近几年科学家发明的一种新型可控电池——锂水电池,工作原理如图所示。下列有关说法不正确的是( )

A. 石墨极发生的反应是2H2O+2e— === H2↑+2OH—
B. 有机电解质和水溶液不可以互换区域
C. 该装置不仅可提供电能,还可得到清洁的氢气
D. 标准状况下产生22.4 L的氢气时,正极消耗锂的质量为14 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验: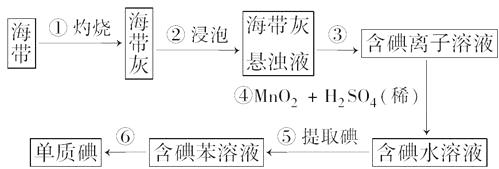
请填写下列空白:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的仪器是()。(从下列仪器中选择所需的仪器,用标号字母填写在空白处)
A.烧杯
B.坩埚
C.表面皿
D.泥三角
E.酒精灯
F.干燥器
(2)步骤③的实验操作名称是;步骤⑥的目的是从含碘苯溶液中分离出碘和回收苯,该步骤的实验操作名称是。
(3)步骤④反应的离子方程式是。
(4)步骤⑤中,某学生选择用苯来提取碘的理由是?
(5)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列装置的说法不正确的是( ) 
A.装置①是原电池,装置②是电镀池
B.装置①中盐桥内的K+移向CuSO4溶液
C.装置①②铜极均发生氧化反应而溶解
D.装置②中的Cu2+浓度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废水中含有CN-和Cr2O72-等离子,需经污水处理达标后小能排放,污水处理拟采用下列流程进行处理:
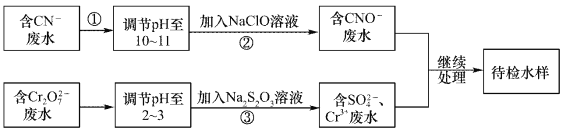
回答下列问题:
(1)步骤②中,CN-被ClO-氧化为CNO-的离子方程式为____________。
(2)步骤③的反应的离了方程式为S2O32-+Cr2O72-+H+→SO42-+Cr3++H2O(未配平),每消耗0.4mol Cr2O72-时,反应中S2O32-失去_________mol电子。
(3)含Cr3+废水可以加入熟石灰进一步处理,目的是___________________。
【答案】 CN-+ClO- = CNO-+Cl- 2.4 调节废水pH,使其转化为Cr(OH)3沉淀除去
【解析】(1)步骤②中,CN-被ClO-氧化为CNO-,因为是在碱性环境中,所以ClO-只能被还原为Cl-,因此反应的离子方程式为CN-+ClO- = CNO-+Cl-;(2)根据方程式可知,在反应中Cr元素的化合价从+6价降低到+3价,得到3个电子,所以0.4 mol Cr2O72-转化为Cr3+时转移电子的物质的量=0.4mol×(6-3)×2=2.4mol;(3)熟石灰是强碱,溶于水显碱性,所以含Cr3+废水中加入熟石灰进一步处理的目的是调节废水pH,使其转化为Cr(OH)3沉淀除去。
【题型】综合题
【结束】
30
【题目】用湿法制磷酸的副产品氟硅酸(H2SiF6)生成无水氟化氢的工艺如图所示:
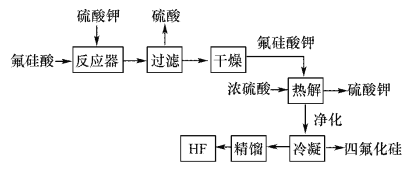
已知氟硅酸钾(K2SiF6)微酸性,有吸湿性,微溶于水,不溶于酒精。
(1)写出反应器中的化学方程式:________________。
(2)在实验室过滤操作中所用的玻璃仪器有_____________,在洗涤氟硅酸钾(K2SiF6)时常用酒精洗涤,其目的是:____________。
(3)该流程中哪些物质可以循环使用:_____________。(用化学式表达)
(4)氟化氢可以腐蚀刻画玻璃,在刻蚀玻璃过程中也会生成H2SiF6,试写出该反应的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒液流电池是一种新型的绿色环保储能电池.其电池总反应为:
V3++VO2++H2O ![]() VO2++2H++V2+ , 下列说法正确的是( )
VO2++2H++V2+ , 下列说法正确的是( )
A.放电时每转移2mol电子时,消耗1mol氧化剂
B.放电时正极反应为:VO+2+2H++e﹣=VO2++H2O
C.放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极
D.充电过程中,H+由阴极区移向阳极区迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去括号内杂质所用试剂和方法不正确的是( )
A. KNO3(NaCl)——结晶
B.水(酒精)——分液
C.Cu(Fe)——溶于足量盐酸,过滤
D. CO2(HCl)——饱和碳酸氢钠溶液,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如右图的反应关系:

(1)若A是淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质。写出其中D与水反应生成的酸名称___________________。
(2)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。写出③反应的化学方程式_____________________。
(3)若D物质具有两性,②③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。写出④反应离子方程式______________________。
(4)若A是应用最广泛的金属,④反应用到A,②⑤反应均用刭同一种非金属单质。写出反应④的离子方程式______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com