
【题目】Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为:
Ca(ClO)2+4HCl(浓)=CaCl2+2Cl2↑+2H2O
回答下列问题:
(1)浓盐酸在反应中显示出来的性质是________(填字母)。
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)产生0.3 mol Cl2,则转移的电子的物质的量为____________mol。
(3)此反应的离子方程式为_____________________。
(4)用双线桥法标出该反应的电子转移的方向和数目:_________________________。
(5)配平化学方程式:______KMnO4+_______HC1(浓)=_______KCl+_______MnCl2+_______Cl2↑+______H2O
【答案】(1)B;(2)0.3;(3)ClO-+Cl-+2H+=C12↑+H2O;
(4)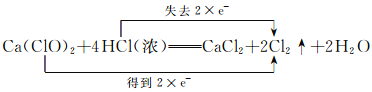 ;
;
(5)2,16,2 ,2 ,5 ,8 。
【解析】
试题分析:(1)浓盐酸中一部分Cl失去电子转化成Cl2,表现还原性,一部分表现酸性,转化成CaCl2,故选项B正确;(2)生成2mol氯气时,转移的物质的量2mol电子,因此生成0.3mol氯气转移电子物质的量为0.3×2/2mol=0.3mol;(3)此反应的离子反应方程式为:ClO- +Cl- +2H+=C12↑+H2O;(4)根据(2)中分析,ClO2-得到电子转化成氯气,因此双线桥的表示形式是:
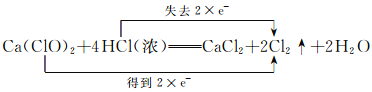 ;
;
(5)KMnO4中Mn由+7价→+2价,化合价降低5价,HCl中Cl-由-1价→0,化合价升高1价,最小公倍数为5,然后根据原子守恒,配平其他,即2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O。


科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.硫氰化钾溶液与氯化铁溶液反应:3SCN-+Fe3+![]() Fe(SCN)3↓
Fe(SCN)3↓
B.氧气通入稀硫酸酸化的KI溶液:O2+2 H2O+4I-=2I2+4OH-
C.酸性高锰酸钾溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+==2Mn2++8H2O+10CO2↑
D.向盐酸中逐滴加入等体积等浓度的碳酸钠溶液:CO32-+2H+==CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种新型自来水消毒剂,实验室可通过以下反应制得ClO2:
2 KC1O3+H2C2O4+H2SO4 ![]() 2 ClO2↑+K2SO4+2CO2↑+2H2O
2 ClO2↑+K2SO4+2CO2↑+2H2O
下列说法正确的是( )
A.KClO3在反应中失电子
B.ClO2是氧化产物
C.H2C2O4在反应中被氧化
D.每消耗1 mol KClO3,转移电子的物质的量为2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关中和滴定的部分操作顺序正确的是( )
① 标准溶液润洗滴定管;② 往滴定管中注入标准溶液;③ 检查滴定管是否漏水;④ 滴定;⑤ 洗涤滴定管;⑥ 调整滴定管中液面在“0”或“0”以下刻度;⑦记数。
A.⑤①②③④⑥⑦ B.③⑤①②⑥⑦④ C.③⑤②⑦①⑥④ D.②⑥⑦①③⑤④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示: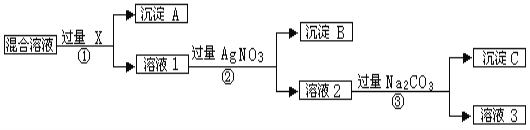
请回答下列问题:
(1)写出实验流程中下列物质的化学式:
试剂X_____________,沉淀A____________,沉淀B______________;
(2)上述实验流程中加入过量的Na2CO3的目的是____________________________。
(3)按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________(填化学式),之后若要获得固体NaNO3需进行的实验操作是__________________________(填操作名称)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在溶液导电性实验装置里,分别注入20mL 6mol·L-1醋酸和20mL 6mol·L-1氨水,灯光明暗
程度相似,如果把这两种溶液混和后再试验则( )
A.灯光明暗程度不变 B.灯光变暗
C.灯光明暗程度变化不明显 D.灯光变亮
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于组成生物体的化学元素的叙述中,正确的是
A. 组成细胞的化学元素在无机环境中都能找到
B. 细胞鲜重中含量最多的元素是碳元素,其次是氧元素
C. 组成生物体的化学元素有些是生物体特有的
D. 微量元素不但含量少,其作用也小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)试分析下列各种情况下微粒间作用力的变化情况,用“离子键”“极性键”或“非极性键”填空:
①NaCl溶于水时被破坏的是 。
②HCl溶于水时被破坏的是 。
③Na2O熔化时被破坏的是 。
④NaOH和HCl反应时形成 和 。
⑤反应2H2+O2![]() 2H2O中,被破坏的是 ,形成的是 。
2H2O中,被破坏的是 ,形成的是 。
⑥Ca(OH)2和NH4Cl反应时,被破坏的化学键有 ,形成的化学键有 。
(2)下列反应过程中,同时有离子键、极性键和非极性键的断裂和形成的反应是 (填字母)。
A.NH4Cl=NH3↑+HCl↑
B.NH3+CO2+H2O=NH4HCO3
C.2NaOH+Cl2=NaCl+NaClO+H2O
D.2Na2O2+2CO2=2Na2CO3+O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com