
【题目】关于化合物![]() 的结构简式如图
的结构简式如图![]() 的说法正确的是
的说法正确的是
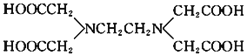
A.![]() 中所含的化学键有离子键、共价键、配位键和氢键
中所含的化学键有离子键、共价键、配位键和氢键
B.EDTA中碳原子的杂化轨道类型为![]() 、
、![]()
C.![]() 的组成元素的第一电离能顺序为
的组成元素的第一电离能顺序为![]()
D.![]() 与
与![]() 互为等电子体,但空间构型不同
互为等电子体,但空间构型不同
【答案】B
【解析】
本题考查化学键类型、杂化方式、第一电离能和等电子体的判断,运用化学键类型、杂化方式、第一电离能和等电子体的判断方法分析。
A.![]() 中所含的化学键有硫酸根离子与配离子之间是离子键,硫酸根离子、EDTA内部是共价键,EDTA与铜离子之间是配位键,氢键不属于化学键,故A错误;
中所含的化学键有硫酸根离子与配离子之间是离子键,硫酸根离子、EDTA内部是共价键,EDTA与铜离子之间是配位键,氢键不属于化学键,故A错误;
B.EDTA中有6个“—CH2—”和4个“—COOH”,“—CH2—”中碳原子为![]() 杂化,“—COOH”中碳原子为
杂化,“—COOH”中碳原子为![]() 杂化,所以EDTA中碳原子的杂化轨道类型为
杂化,所以EDTA中碳原子的杂化轨道类型为![]() 、
、![]() ,故B正确;
,故B正确;
C.同一主族中,从上向下,元素第一电离能逐渐减小,同一周期中,元素的第一电离能随着原子序数的增大呈增大趋势,但N原子最外层的2p能级处于半满状态,是一种较稳定结构,所以它的第一电离能高于同周期相邻的元素,![]()
![]() 的组成元素的第一电离能顺序为
的组成元素的第一电离能顺序为![]() ,故C错误;
,故C错误;
D.![]() 中S原子价层电子对数
中S原子价层电子对数![]() ,没有孤电子对,故
,没有孤电子对,故![]() 为正四面体结构,
为正四面体结构,![]() 与
与![]() 互为等电子体,
互为等电子体,![]() 也正四面体结构,故D错误;
也正四面体结构,故D错误;
答案选B。


科目:高中化学 来源: 题型:
【题目】下列热化学方程式(△H的绝对值均正确)书写正确的是 ( )
A.2CO(g)+O2(g)===2CO2(g); ![]() H=-566 kJ·mol-1(燃烧热)
H=-566 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq) ===NaCl(aq)+H2O(l); ![]() H=+57.3 kJ·mol-1 (中和热)
H=+57.3 kJ·mol-1 (中和热)
C.C2H5OH(l)+3O2(g) ===2CO2(g)+3H2O(l);![]() H=-1366.8 kJ·mol-1 (燃烧热)
H=-1366.8 kJ·mol-1 (燃烧热)
D.Ba(OH)2(aq)+2HCl(aq)===BaCl2(aq)+2H2O(l);![]() H=-114.6 kJ·mol-1 (中和热)
H=-114.6 kJ·mol-1 (中和热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸式盐NaHB在水溶液中存在下列变化:①NaHB===Na++HB-,②HB-![]() H++B2-,③HB-+H2O
H++B2-,③HB-+H2O![]() H2B+OH-,且溶液中c(B2-)>c(H2B),则下列说法一定正确的是( )
H2B+OH-,且溶液中c(B2-)>c(H2B),则下列说法一定正确的是( )
A. 0.01 mol·L-1的NaHB溶液,其pH可能为2
B. NaHB及H2B均为强电解质
C. 该酸式盐溶液中水电离出的氢离子浓度小于纯水中水电离出的氢离子浓度。
D. HB-的电离程度小于HB-的水解程度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.在一定温度下的恒容容器中,当下列物理量不再发生变化时,不能表明反应: A(s)+3B(g)![]() 2C(g)+D(g)已达平衡状态的是
2C(g)+D(g)已达平衡状态的是
A. 混合气体的压强B. 混合气体的密度
C. 3v逆(C)=2v正(B)D. 气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于价电子构型为![]() 的原子描述正确的是
的原子描述正确的是
A.它的核外电子排布式为![]()
B.它的最高能级轨道上有2对电子对
C.它有34种不同运动状态的电子
D.它的第二电离能小于As
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y是同周期的主族元素,且电负性大小:![]() 。下列说法错误的是
。下列说法错误的是
A.X与Y形成的化合物中,X显负价,Y显正价
B.第一电离能可能Y小于X
C.X的最高价含氧酸酸性弱于Y的
D.气态氢化物的稳定性:![]() 小于
小于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法中,正确的是
①在家庭中用食醋和碘化钾淀粉试纸检验食盐是否是加碘![]() 盐
盐
②用酒精从碘水中萃取碘
③用加热的方法从碘和沙子的混合物中分离出碘
④实验室制![]() 、
、![]() 都用同一套装置
都用同一套装置
⑤用淀粉溶液直接检验![]()
⑥根据加入![]() 溶液产生白色沉淀的现象认定溶液中含
溶液产生白色沉淀的现象认定溶液中含![]()
⑦盛放液溴的试剂瓶内放少量蒸馏水防止液溴的挥发
⑧用溴水鉴别![]() 和
和![]()
A.①②③⑧B.③④⑥⑦C.①③⑦⑧D.②④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常把原子总数和价电子总数相同的分子或离子称为等电子体.人们发现等电子体的空间结构相同,则下列有关说法中正确的是
A.![]() 和
和![]() 是等电子体,键角均为
是等电子体,键角均为![]()
B.![]() 和
和![]() 是等电子体,均为平面正三角形结构
是等电子体,均为平面正三角形结构
C.![]() 和
和![]() 是等电子体,均为三角锥形结构
是等电子体,均为三角锥形结构
D.![]() 和苯是等电子体,
和苯是等电子体,![]() 分子中不存在“肩并肩”式重叠的轨道
分子中不存在“肩并肩”式重叠的轨道
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com