
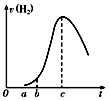
 某浓度的硫酸中投入2.5g在空气中久置的铝片,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图来表示,下列叙述不正确的是( )
某浓度的硫酸中投入2.5g在空气中久置的铝片,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图来表示,下列叙述不正确的是( )| A. | O→a不产生氢气是因为氧化铝和硫酸反应 | |
| B. | b→c产生氢气的速率增大较快的主要原因之一是温度升高 | |
| C. | t=c时反应处于平衡状态 | |
| D. | t>c产生氢气的速率减小主要是因为溶液中的c(H+)降低 |
分析 由图可知,开始不生成氢气,为氧化铝与硫酸的反应,然后Al与硫酸反应生成氢气,开始温度较低,由于反应放热,则温度升高反应速率加快,后来,氢离子浓度减小,则反应速率减小,以此来解答.
解答 解;A.曲线由0→a段不产生氢气是因表面的氧化物隔离了铝和硫酸溶液,氧化铝与硫酸反应生成硫酸铝和水,离子反应为Al2O3+6H+=2Al3++3H2O,故A正确;
B.曲线由b→c段,产生氢气的速率增加较快的主要原因为该反应为放热反应,温度升高,反应速率加快,故B正确;
C.反应不是可逆反应,随反应进行反应放热对速率的影响比浓度减少的影响大,当t=c时温度影响最大,t>c时温度影响不是主要因素,浓度减少是主要因素,故C错误;
D.曲线由c以后,产生氢气的速率逐渐下降的主要原因为氢离子浓度减小,反应速率减小,故D正确.
故选C.
点评 本题考查Al的化学性质及影响反应速率的因素,为高频考点,把握温度、浓度对反应速率的影响及氧化铝、Al与酸的反应为解答的关键,侧重分析能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 都是混合物 | |
| B. | 前者主要含甲烷,后者主要含丙烷、丁烷 | |
| C. | 主要成分都是烷烃 | |
| D. | 常温常压下,前者呈气态,后者呈液态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁上镀锌的保护方法叫牺牲负极的正极保护法 | |
| B. | 相同条件下,轮船在海水中比在淡水中腐蚀慢 | |
| C. | 钢铁在潮湿的空气中会发生吸氧腐蚀,负极反应为Fe-3e-=Fe3+ | |
| D. | 水库里钢闸门与电源负极相连的方法叫做外加电流的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
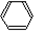 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$ -NO2+H2O.
-NO2+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

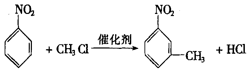 .
.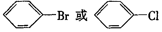 ,②
,② .
. 的所有原子不是(填“是”或“不是”)在同一平面上.
的所有原子不是(填“是”或“不是”)在同一平面上.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com