
| A、石油 | B、煤 | C、天然气 | D、乙醇 |
科目:高中化学 来源: 题型:
| A、杂质一定不含KNO3 |
| B、杂质一定含有Ba(NO3)2可能还含有KNO3 |
| C、杂质一定不含Na2SO4 |
| D、杂质一定含KNO3可能还含有Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、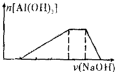 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 SiH4(硅烷)法生产高纯多晶硅是非常优异的方法.
SiH4(硅烷)法生产高纯多晶硅是非常优异的方法.查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,设A池中原混合液的体积为200mL.
如图所示,通电5min后,第③极增重2.16g,同时在A池中收集到标准状况下的气体224mL,设A池中原混合液的体积为200mL.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相同温度下,溶液中水的电离程度:溶液①>溶液② | ||
| B、等体积混合溶液①和溶液②,所得溶液中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | ||
C、加水稀释溶液①,溶液中
| ||
D、向溶液①中加少量的CH3COONa固体则
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | A-A | B-B | A-B |
| 生成1mol化学键时放出的能量 | 436kJ?mol-1 | 243kJ?mol-1 | 431kJ?mol-1 |
A、
| ||||
| B、A2(g)+B2(g)═2AB(g)△H=-183kJ?mol-1 | ||||
C、
| ||||
| D、2AB(g)═A2(g)+B2(g))△H=+183kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
A、将NH4+转化为NO3-的热化学方程式可表示为:NH4+(aq)+2O2(g)═NO3-+2H+(aq)+H2O(l)△H=-(b+
| ||
| B、在上述两次转化过程中,废水的酸性先增大然后逐渐减弱 | ||
| C、常温下,若HNO2溶液中c(H+)=0.1 mol?L-1,则该溶液的pH>1 | ||
| D、若上述两次转化完全,不考虑其它杂质离子的存在,则:c(NH4+)+c(OH-)═c(NO3-)+c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com