
| A. | 它们都属于混合物 | B. | 它们都是乙烯的同系物 | ||
| C. | 它们的分子都不含氢原子 | D. | 聚四氟乙烯分子中含有双键 |
分析 四氯乙烯为CCl2=CCl2,四氟乙烯为CF2=CF2,CF2=CF2发生加聚反应可生成聚四氟乙烯,聚四氟乙烯不含碳碳双键,以此解答该题.
解答 解:A.四氯乙烯为CCl2=CCl2,属于纯净物,聚四氟乙烯属于高聚物,为混合物,故A错误;
B.四氯乙烯、聚四氟乙烯与乙烯的分子组成不同,则它们一定不属于同系物,故B错误;
C.四氯乙烯、四氟乙烯的结构简式分别为CCl2=CCl2、CF2=CF2,CF2=CF2发生加聚反应可生成聚四氟乙烯,二者分子中都被还原H原子,故C正确;
D.CF2=CF2发生加聚反应可生成聚四氟乙烯,不含碳碳双键,故D错误.
故选C.
点评 本题考查了卤代烃的组成与结构的判断,侧重化学与生活的考查,题目难度不大,注意掌握常见有机物组成、结构及性质,明确同系物、纯净物的概念为解答关键.


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | pH<5.6降水通常称为酸雨;CO2的大量排放能破坏臭氧层,形成“臭氧空洞” | |
| B. | 总质量一定时,乙酸和葡萄糖无论以何种比例混合,完全燃烧消耗氧气的量相等 | |
| C. | 燃煤时加入适量石灰石,可减少废气中SO2的量 | |
| D. | 有机高分子化合物称为聚合物或高聚物,是因为他们大部分是由小分子通过聚合反应制得的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石灰水 | B. | 豆浆 | C. | 泥水 | D. | 蔗糖水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ③④⑤ | C. | ①③⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 6 种 | C. | 8种 | D. | 10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将磁性氧化铁溶于稀硫酸:Fe3O4+8H+=3Fe3++4H2O | |
| B. | 0.2mol明矾与300mL1mol/L的氢氧化钡溶液混合:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ | |
| C. | 将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑ | |
| D. | 将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
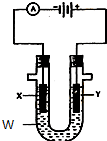 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液w;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液w;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com