
【题目】硼氢化钠(NaBH4)在化工领域具有重要的应用价值,可采用硼砂、SiO2、Na和H2作为原料制备。回答下列问题:
(1)周期表中,与B的化学性质最相似的邻族元素是____;该元素基态原子核外M层电子中自旋状态相同的有_____个。
(2)NaBH4中,电负性最大的元素是____(填元素符号);B的____杂化轨道与H的1s轨道形成![]() 键。
键。
(3)硼砂是含8个结晶水的四硼酸钠。其阴离子(含B、O、H三种元素)的球模型如图所示:
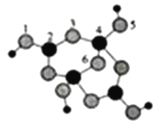
①阴离子中,配位键存在于____和____原子之间。(均填原子的序号)
②硼砂的化学式为_______。
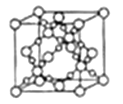
(4)SiO2晶胞(立方体)如图所示,已知SiO2的密度为![]() g/cm3,设阿伏加德罗常数的值为NA,则SiO2晶胞的边长为___pm。
g/cm3,设阿伏加德罗常数的值为NA,则SiO2晶胞的边长为___pm。
【答案】Si 3 H sp3 4 5 Na2B4O5(OH)4·8H2O 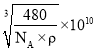
【解析】
(1)在周期表中,与B的化学性质最相似的邻族元素是Si,硅元素基态原子核外M层电子排布式为3s23p2,所以有3个电子的自旋状态相同;
(2)电负性规律:同周期,从左到右:电负性依次增大;同主族,从上到下:电负性依次减小。NaBH4中电负性最大的元素为H;依据价层电子理论,NaBH4中B的价层电子对数为4,为sp3杂化。
(3)①1,3,5,6代表氧原子,2,4代表B原子,2号B形成3个键,则B原子为SP2杂化,4号B形成4个键,则B原子为SP3杂化;B一般是形成3个键,4号B形成4个键,其中1个键很可能就是配位键,配位键存在4号与5号之间;
②硼砂晶体由Na+、含有B的阴离子和H2O构成。观察模型,可知含有B的阴离子是(H4B4O9)m,依据化合价H为+1,B为+3,O为2,可得m=2,结合模型图和组成,硼砂的化学式为Na2B4O5(OH)4·8H2O;
(4)SiO2晶胞中,大球是Si,小球是O。Si的数目为![]() ,O是Si的2倍,故是16。晶体的密度
,O是Si的2倍,故是16。晶体的密度![]() ,晶胞的体积V=a3。因此SiO2晶胞的边长a=
,晶胞的体积V=a3。因此SiO2晶胞的边长a=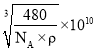 。
。


 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理(平衡移动原理)解释的是
A. 对于反应体系 CO(g) + NO2(g) ![]() NO(g) + CO2(g),压缩体积可使颜色变深
NO(g) + CO2(g),压缩体积可使颜色变深
B. 实验室可用排饱和食盐水的方法收集氯气
C. 重铬酸钾溶液中存在如下平衡:Cr2O72-(橙红色)+H2O![]() 2H++2CrO42-(黄色),向K2Cr2O7溶液中加入几滴氢氧化钠,溶液变黄色
2H++2CrO42-(黄色),向K2Cr2O7溶液中加入几滴氢氧化钠,溶液变黄色
D. 开启啤酒瓶后,瓶中马上泛起大量泡沫
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)难溶物PbSO4溶于CH3COONH4溶液可制得易溶于水的(CH3COO)2Pb,发生的反应为PbSO4+2CH3COONH4=(CH3COO)2Pb+(NH4)2SO4,说明(CH3COO)2Pb是________(填“强”或“弱”)电解质。
(2)已知次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成NaH2PO2和H2O,则次磷酸是_____元酸(填“一”、“二”或“三”)。
(3)工业上制玻璃和水泥需用到的共同原料是________(填化学式)。
(4)在一定温度下,向一个2 L的真空密闭容器中(预先装入催化剂)通入1 mol N2和3 mol H2,发生反应:N2(g)+3H2(g)2NH3(g)。经过一段时间后,测得容器内压强是起始的0.9倍,在此时间内,H2平均反应速率为0.1 mol/(L·min),则所经过的时间为______min
(5)高铁酸钠(Na2FeO4)具有强氧化性,可对自来水进行消毒、净化。高铁酸钠可用氢氧化铁和次氯酸钠在碱性介质中反应得到,请补充并配平下面离子方程式。
____Fe(OH)3 +____ClO-+____OH-=__FeO42-+___Cl-+__
(6)在反应11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4中,氧化剂是___________;当有2mol H3PO4生成,转移的电子的物质的量为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA 为阿伏加德罗常数,下列说法正确的是
A. 标准状况下,11.2L CCl4 中含 C—Cl 键的数目 1.5NA
B. 8.7g MnO2 与 40 mL 10 mol·L-1的浓盐酸充分反应,生成的氯气分子数为 0.1 NA
C. 1mol NaHSO4固体中含有的离子总数为 2 NA
D. 0.5mol·L-1K2SO4 溶液中,阴阳离子总数为 1.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用该浓硫酸配制100 mL 1 mol/L的稀硫酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。请回答下列问题:
(1)配制稀硫酸时,上述仪器中不需要使用的有__________(填序号),还缺少的仪器有____________________(写仪器名称);
(2)经计算,配制100mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为____________________________________________mL(保留一位小数),量取浓硫酸时应选用_________(选填10mL、50mL 、100mL)规格的量筒;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钾溶液常用作利尿剂及防治缺钾症的药物,某医疗实验小组需要用到480 mL物质的量浓度为0.5 mol·L-1的氯化钾溶液。回答下列问题:
(1)配制该溶液,需称量氯化钾晶体的质量是________。
(2)配制上述氯化钾溶液,需要使用的玻璃仪器是量筒、烧杯、玻璃棒、________、________。
(3)如图Ⅰ表示10 mL量筒中液面的位置,刻度A与B,B与C间均相差1 mL,如果刻度A为9,则量筒中液体的体积是________mL。

(4)定容时,某同学操作示意图如图Ⅱ所示,则其所配氯化钾溶液的浓度________(填“大于”“等于”或“小于”)0.5 mol·L-1;某同学由于操作不慎,定容时导致液面高于刻度线,他立即用胶头滴管将液体吸出,使液面恰好达到刻度线,请你评价该同学的做法:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在 2 L 密闭容器中,A、B、C 三种气体的物质的量随时间变化的曲线如图所示。下列说法正确的是( )
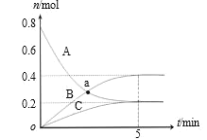
A.反应开始到 5min,υ(C)=0.2 mol/(L·min)
B.反应开始到 5min,B 的物质的量浓度增加了 0.4 mol/L
C.反应的化学方程式为:2B(g)+C(g)![]() 3A(g)
3A(g)
D.a 点时,c(A)=c(B)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com