

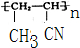
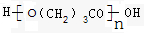
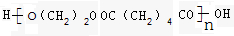 .
. 分析 (1)含碳碳双键的有机物可发生加聚反应;
(2)同时含-OH和-COOH的有机物本身可发生缩聚反应;
(3)含2个-OH的有机物与含2个-COOH的有机物可发生缩聚反应.
解答 解:(1)含碳碳双键的有机物可发生加聚反应,只有c符合,则加聚物的结构简式为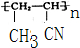 ,故答案为:c;
,故答案为:c;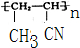 ;
;
(2)同时含-OH和-COOH的有机物本身可发生缩聚反应,只有a符合,缩聚物的结构简式为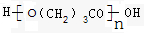 ,
,
故答案为:a;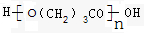 ;
;
(3)含2个-OH的有机物与含2个-COOH的有机物可发生缩聚反应,则b、e可发生缩聚反应,所得产物的结构简式为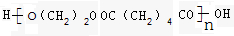 ,
,
故答案为:b;e;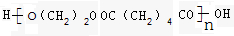 .
.
点评 本题考查有机物的结构与性质,为高频考点,侧重加聚反应与缩聚反应的考查,把握官能团与性质的关系及合成高分子化合物的反应为解答的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 N、P、As、Ga、Cr等元素化合物种类繁多,具有重要的研究价值和应用价值.请回答下列问题:
N、P、As、Ga、Cr等元素化合物种类繁多,具有重要的研究价值和应用价值.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12种 | B. | 11种 | C. | 9种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 器材和试剂 | 相应实验 |
| A | 洗气瓶,饱和Na2CO3溶液、浓硫酸、含HCl和水蒸气的CO2气体 | 除去CO2中的HCl和水蒸气 |
| B | 分液漏斗、烧杯、蒸馏水、溴和苯的混合物 | 分离溴和苯的混合物 |
| C | 铁架台、试管、带导管的单孔塞、浓硫酸、铜片 | 实验室制取SO2 |
| D | 铁架台、试管、带导管的单孔塞、棉花、酒精灯、氯化铵晶体、熟石灰 | 实验室制取NH3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (用电子式表示).
(用电子式表示).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 | |
| C. | 1.00 mol NaCl中含有6.02×1023个NaCl分子 | |
| D. | 纯净矿泉水、铝热剂、漂白粉均为混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 把浓硝酸放在棕色瓶中,并置于冷暗处保存 | |
| B. | 把Na保存在煤油中 | |
| C. | 把NaOH溶液放在带橡皮塞的玻璃瓶中 | |
| D. | 把氢氟酸放在玻璃瓶中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com