
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:2PbSO4+2H2O Pb+PbO2+2H2SO4则下列说法正确的是( )
Pb+PbO2+2H2SO4则下列说法正确的是( )
|
| A. | 放电时,该电池的正极材料是硫酸铅 |
|
| B. | 充电时,阳极反应是:PbSO4﹣2e﹣+2H2O=PbO2+SO42﹣+4H+ |
|
| C. | 充电时,电池中硫酸的浓度不断减小 |
|
| D. | 放电时,正极反应是:Pb﹣2e﹣+SO42﹣=PbSO4 |
考点:
常见化学电源的种类及其工作原理.
专题:
电化学专题.
分析:
由铅蓄电池的总反应:2PbSO4+2H2O Pb+PbO2+2H2SO4可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb﹣2e﹣+SO42﹣=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42﹣+2e﹣+4H+═PbSO4+2H2O,在充电时,阳极上发生氧化反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应,以此解答.
Pb+PbO2+2H2SO4可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb﹣2e﹣+SO42﹣=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42﹣+2e﹣+4H+═PbSO4+2H2O,在充电时,阳极上发生氧化反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应,以此解答.
解答:
解;A.放电时,正极上PbO2得电子被还原,该电池的正极材料是PbO2,故A错误;
B.在充电时,阳极上发生氧化反应,和放电时的正极反应互为逆反应,即PbSO4﹣2e﹣+2H2O=PbO2+SO42﹣+4H+,故B正确;
C.充电时,反应总方程式为2PbSO4+2H2O=Pb+PbO2+2H2SO4,生成硫酸,硫酸浓度不变增大,故C错误;
D.放电时,正极上PbO2得电子被还原,电极反应式为PbO2+SO42﹣+2e﹣+4H+═PbSO4+2H2O,故D错误.
故选B.
点评:
本题考查了原电池和电解池原理,明确正负极、阴阳极上得失电子及电极反应是解本题关键,难点是电极反应式的书写,注意原电池正负极上发生的反应为电解池阳极、阴极上发生反应的逆反应,难度中等.


科目:高中化学 来源: 题型:
PtCl2(NH3)2可以形成两种固体,一种为淡黄色,在水中的溶解度较小,另一种为黄绿色,在水中的溶解度较大。请回答下列问题:
(1)PtCl2(NH3)2是平面正方形结构,还是四面体结构? 。
(2)请在横线上画出这两种固体分子的几何构型图:
①淡黄色固体: ②黄绿色固体: 。
(3)淡黄色固体物质由 分子组成,黄绿色固体物质由 分
子组成(填“极性”或“非极性”)。
(4)黄绿色固体在水中的溶解度比淡黄色固体的大,原因是
________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求完成下列各题:
(1)用电子式表示Mg Cl2的形成过程.H2O的电子式为.
(2)质量相同的H2O和D2O所含质子数之比为.
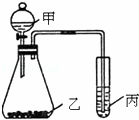
(3)利用如图装置采用适当试剂可完成某探究实验,并得出相应实验结论.请根据相关信息回答:
①为了证明元素的非金属性强弱是S>C>Si.你认为各物质应该是:甲为硫酸;乙为;丙为.(已知乙中有气泡产生,丙中有白色沉淀)
②如果甲为水,乙为Na2O2粉末,丙为H2S的饱和水溶液.实验中观察到丙中生成淡黄色沉淀.说明元素O、S非金属性强弱为.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作中,能使电离平衡H2O⇌H++OH﹣,向右移动且溶液呈酸性的是( )
|
| A. | 向水中加入NaHSO4溶液 | B. | 向水中加入Al2(SO4)3溶液 |
|
| C. | 向水中加入NaOH溶液 | D. | 将水加热到100℃,使pH=6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
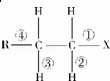
在卤代烃R﹣CH2﹣CH2﹣X中化学键如图所示,则下列说法正确的是( )
|
| A. | 发生水解反应时,被破坏的键是①和③ |
|
| B. | 发生消去反应时,被破坏的键是②和③ |
|
| C. | 发生水解反应时,被破坏的键是① |
|
| D. | 发生消去反应时,被破坏的键是①和② |
查看答案和解析>>
科目:高中化学 来源: 题型:
我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图:
气体A的饱和溶液 A和食盐的饱和溶液
A和食盐的饱和溶液 悬浊液
悬浊液 晶体
晶体 纯碱
纯碱
则下列叙述错误的是()
A. A气体是CO2,B气体是NH3
B. 第Ⅲ步得到的晶体是发酵粉的主要成分
C. 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D. 第Ⅳ步操作的主要过程有溶解、蒸发、结晶
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中评价不合理的是 ( )。
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | 向碳酸镁中加入稀盐酸:CO | 错误,碳酸镁不应写成离子形式 |
| B | 向硫酸铜溶液中加入氢氧化钡溶液:Ba2++SO | 正确 |
| C | 向FeCl3溶液中加入Fe粉:Fe3++Fe===2Fe2+ | 错误,离子所带电荷不守恒且电子得失不相等 |
| D | 以石墨作电极电解氯化钠溶液:2Cl-+2H2O | 正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com