
把下列四种X溶液分别加入四个盛有10mL 2mol/L盐酸的烧杯中,均加水稀释到50mL,此时,X和盐酸缓慢地进行反应,其中反应最快的是( )
A.10℃20mL 3mol/L的X溶液 B.20℃30mL 2mol/L的X溶液
C.20℃10mL 4mol/L的X溶液 D.10℃10mL 2mol/L的X溶液
科目:高中化学 来源: 题型:
某温度时,水的离子积为1.0×12-12,由此可知在该温度时纯水电离的c(H+)为
A. 1.0×12-7 B. 1.0×12-2 C. 1.0×12-6 D. 1.0×12-14
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g)===2HF(g) 的能量变化如图所示,下列有关叙述中正确的是
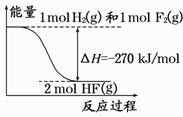
A.氟化氢气体分解生成氢气和氟气的反应是放热反应
B.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
C.在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
D.断裂1 mol H—H键和1 mol F—F 键放出的能量大于形成2 mol H—F键放出的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质分类的说法正确的是( )
A. 化合反应均为氧化还原反应
B. 液氨、液氯、液体氯化氢都是非电解质
C. 多糖、油脂、蛋白质都是高分子化合物
D. 古代的陶瓷、砖瓦,现代的玻璃、水泥等,都是硅酸盐产品
查看答案和解析>>
科目:高中化学 来源: 题型:
生产自来水的流程如图所示:回答下列问题。
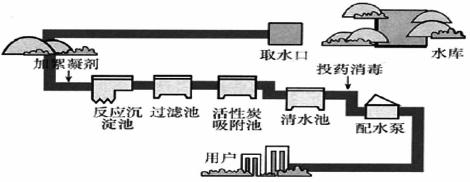
(1)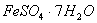 是常用的絮凝剂,它在水中最终生成__________沉淀(填化学式)。
是常用的絮凝剂,它在水中最终生成__________沉淀(填化学式)。
(2)天然水中含有较多的钙、镁离子,称为硬水。生活中常用__________方法来降低水的硬度。
(3)过滤池利用了实验室过滤原理,在实验室过滤操作所用到的玻璃仪器是__________。
(4)“投药消毒”中的“药”指漂白粉,请写出制取漂白粉的化学方程式__________。
(5)水的电离平衡曲线如图所示,若A点表示25℃时水的电离达平衡时的离子浓度,B点表示100℃时水的电离达平衡时的离子浓度。
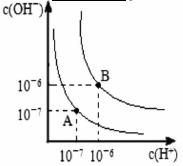
①100℃时1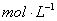 的NaOH溶液中,由水电离出的c(H+)=________
的NaOH溶液中,由水电离出的c(H+)=________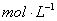 ,Kw(25℃)__________Kw(100℃)(填“>”“<”或“=”)。
,Kw(25℃)__________Kw(100℃)(填“>”“<”或“=”)。
②25℃时,向含100ml水的烧杯中逐渐加入一定量的冰醋酸,下列叙述正确的有__________(填字母)。
A. 溶液中一直存在: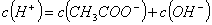
B. 加入过程中,水的电离程度逐渐减小,醋酸的电离程度逐渐增大
C. 加入过程中,溶液中所有离子浓度逐渐增大
D. 加完冰醋酸后,若升高烧杯温度,溶液pH值降低
E. 用已知浓度的NaOH溶液滴定烧杯中的醋酸溶液,测定其浓度,最好选用甲基橙作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
最近科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,另一边附着二氧化锰。电池总反应为Zn+2MnO2+H2O===ZnO+2MnOOH。下列说法不正确的是( )
A.该电池Zn为负极,MnO2为正极
B.该电池的正极反应为MnO2+e-+H2O===MnOOH+OH-
C.导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn
D.电池工作时水分子和OH-都能通过薄层纸片
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=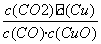
B.反应③的平衡常数K=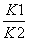
C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应的△H>0
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如图转化关系, 请完成下列问题:
请完成下列问题:
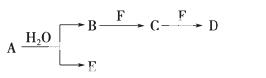
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:_______________________________________________
____________________________________________________________。
②当C为直线形分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为________;D中所含化学键的类型为____________________________
___________________________________ _______________。
_______________。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的相对分子质量相等,请用离子方程式表示F的水溶液呈酸性的原因:______________
___________________ _____________________________________________。
_____________________________________________。
(3)若A中一种元素原子的最外层电子数为内层电子总数的,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:___________________________________________________________________;
B转化为C的化学方程式为____________ ___________________________________。
___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
含有a mol FeBr2的溶液中,通入x mol Cl2。下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是 ( )
A.x=0.4a,2Fe2++Cl2=2Fe3++2Cl-
B.x=0.6a,2Br-+ Cl2=Br2+2Cl-
C.x=a,2Fe2++2Br-+2Cl2=Br2+2Fe3++4Cl-
D.x=1.5a,2Fe2++4Br-+3Cl2=2Br2+2Fe3++6Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com