
 ,则乙炔和水加成的化学方程式是
,则乙炔和水加成的化学方程式是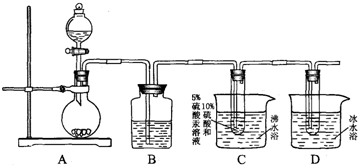
| 催化剂 |
| 催化剂 |
| △ |
| △ |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
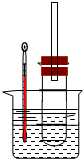 溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物.
溴乙烷在不同溶剂中与NaOH可发生不同类型的反应,生成不同的反应产物.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称取8.0g胆矾使其溶于500mL水中 |
| B、称取12.5g胆矾使其溶于500mL水中 |
| C、称取12.5g胆矾使其溶于适量水中,再加水稀释至500mL. |
| D、称取8.0g胆矾使其溶于375g水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com