
| A | B | C | D | |
图示 |  |  |  |  |
| 结论 | HB为弱酸 | HF为弱电解质 | 溶解度:AgI<AgCl | 正反应△H>0 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.加水稀释相同的倍数弱酸的pH变化小;
B.溶液中存在分子,说明HF没有完全电离;
C.一定条件下,AgCl可以转化为AgI;
D.升高温度K增大,说明向正反应方向移动.
解答 解:A.加水稀释相同的倍数弱酸的pH变化小,HB溶液的pH变化小,所以HB为弱酸,故A正确;
B.溶液中存在分子,说明HF没有完全电离,即HF为弱酸,故B正确;
C.一定条件下,AgCl可以转化为AgI,但是不能说明AgI的溶解度小于AgCl的溶解度,故C错误;
D.升高温度K增大,说明向正反应方向移动,即正反应方向为吸热方向,所以正反应△H>0,故D正确.
故选C.
点评 本题考查了弱电解质的电离、沉淀的转化、温度对化学平衡和平衡常数的影响,题目涉及的知识点较多,侧重于考查学生对基础知识的应用能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 苯在催化剂作用下能与浓硝酸发生取代反应 | |
| B. | 在一定条件下苯能与氢气发生加成反应 | |
| C. | 在苯中加入酸性高锰酸钾溶液,振荡并静置后下层液体为紫红色 | |
| D. | 在苯中加入溴水,振荡后会发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 假设 | B. | 实验 | C. | 做结论 | D. | 观察 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在食用盐中滴加少量淀粉溶液,探究食用盐是否含有IO3- | |
| B. | 新制氯水显酸性,将其滴加到紫色石蕊溶液中,充分振荡后溶液最终为无色 | |
| C. | 氯气具有漂白性,可以将湿润的有色布条漂白为无色物质 | |
| D. | 根据较强酸可以制取较弱酸的规律,结合酸性的强弱顺序H2CO3>HClO>HCO3-,可以推出少量的CO2通入NaClO溶液中能生成HClO和碳酸钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:
(1)已知在常温下,常见弱酸和弱碱的电离平衡常数如下表所示:| 电解质 | HF | CH3COOH | HNO2 | NH3•H2O |
| 电离平衡常数K | 3.53×10-4 | 1.76×10-5 | 4.6×10-4 | 1.77×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定浓度的氨水加水稀释的过程中,c(NH4+)/c(NH3•H2O)的比值减小 | |
| B. | pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)>c(CH3COO -) | |
| C. | 常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在下面关系:c(B-)>c(Na+)>c(HB)>c(H+)>c(OH-) | |
| D. | c(NH4+)相等的(NH4)2SO4、NH4HSO4、NH4Cl溶液中:c(NH4HSO4)>c(NH4)2SO4>c(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 45mL | B. | 180mL | C. | 90mL | D. | 135mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题



 +2H2O.
+2H2O.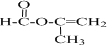 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com