
·ÖĪö £Ø1£©øł¾Ż»Æѧ·“Ó¦·½³ĢŹ½£ŗMnO2+4HCl£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2+2H2O½įŗĻ²śÉśĀČĘųµÄĪļÖŹµÄĮæ½ųŠŠ¼ĘĖć£»
£Ø2£©½«Éś³ÉµÄCl2Ķص½NaOHČÜŅŗÖŠ·¢Éś·“Ó¦£ŗCl2+2NaOHØTNaCl+NaClO+H2O£¬øł¾Żc=$\frac{n}{V}$½ųŠŠ¼ĘĖć£»
£Ø3£©øł¾Ż¶žŃõ»ÆĆĢµÄĮæ¼ĘĖć²Ī¼ÓŃõ»Æ»¹Ō·“Ó¦µÄŃĪĖįµÄĮ棬ÓĆÉś³É³ĮµķµÄĮæ¼ĘĖćČÜŅŗÖŠĀČĄė×ÓµÄĪļÖŹµÄĮ棬ŌŁøł¾ŻŌ×ÓŹŲŗć¼ĘĖćŃĪĖįµÄĪļÖŹµÄĮæÅØ¶Č£®
½ā“š ½ā£ŗ£Ø1£©·“Ó¦½įŹųŹ±ŹÕ¼Æµ½336mLĘųĢåµÄĪļÖŹµÄĮæĪŖ£ŗ$\frac{0.336L}{22.4L/mol}$=0.015mol£¬øł¾Ż·½³ĢŹ½£ŗMnO2+4HCl£ØÅØ£©$\frac{\underline{\;\;”÷\;\;}}{\;}$MnCl2+Cl2”ü+2H2O£¬²śÉś0.015molĀČĘųĻūŗĶžŃõ»ÆĆĢµÄĪļÖŹµÄĮæŹĒ0.015mol£¬ÖŹĮæŹĒ£ŗ0.015mol”Į87g/mol=1.305g£¬“š£ŗ²Ī¼Ó·“Ó¦µÄ¶žŃõ»ÆĆĢµÄÖŹĮæŹĒ1.305g£»
£Ø2£©½«Éś³ÉµÄCl2Ķص½NaOHČÜŅŗÖŠÖʵĆ100mLĻū¶¾Ņŗ£¬·¢Éś·“Ó¦£ŗCl2+2NaOHØTNaCl+NaClO+H2O£¬ÓŠŠ§³É·ÖŹĒNaClO£¬0.015molĀČĘųÄܲśÉś“ĪĀČĖįÄĘŹĒ0.015mol£¬ĖłŅŌc£ØNaClO£©=$\frac{0.015mol}{0.1L}$=0.15mol/L£¬“š£ŗĻū¶¾ŅŗÖŠÓŠŠ§³É·ÖµÄĪļÖŹµÄĮæÅØ¶ČŹĒ0.15mol/L£»
£Ø3£©½«·“Ó¦ŗóµĆµ½µÄ²ŠÓąŅŗ¹żĀĖ”¢Ļ“µÓĀĖŌü£¬Ļ“µÓŅŗŗĶĀĖŅŗ»ģŗĻ£»ĻņĀĖŅŗÖŠ¼ÓČė×ćĮæµÄAgNO3ČÜŅŗ£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļŗóµĆµ½¹ĢĢå11.48g£®¹ĢĢ弓ĪŖAgCl£¬ĪļÖŹµÄĮæŹĒ$\frac{11.48g}{143.5g/mol}$=0.08mol£¬ĖłŅŌČÜŅŗÖŠĀČĄė×ÓµÄĪļÖŹµÄĮæŹĒ0.08mol£¬øł¾ŻMnŹŲŗć£¬²śÉśĀČ»ÆĆĢÖŠĀČĄė×ÓŹĒ0.015mol”Į2=0.03mol£¬ĖłŅŌŃĪĖįŹ£ÓąµÄĮæŹĒ0.05mol£¬
ŃĪĖįŗĶ¶žŃõ»ÆĆĢ·“Ó¦ŗóµÄČÜŅŗÖŠĀČĄė×ÓµÄĪļÖŹµÄĮæµČÓŚĪ“²Ī¼ÓŃõ»Æ»¹Ō·“Ó¦µÄŃĪĖįµÄĪļÖŹµÄĮæ£¬Éś³ÉĀČĘųŹĒ0.015mol£¬“Ė²æ·ÖĄ“×Ō0.03molŃĪĖį£¬ĖłŅŌŌĄ“ŃĪĖįµÄĪļÖŹµÄĮæŹĒ£ŗ0.03mol+0.08mol=0.11mol£¬ÅØ¶ČŹĒ$\frac{0.11mol}{0.012L}$=9.17mol/L£¬
“š£ŗÅØŃĪĖįÄÜŗĶ¶žŃõ»ÆĆĢ·“Ó¦µÄÉś³ÉCl2µÄ×īµĶÅØ¶ČŹĒ9.17mol/L£®
µćĘĄ ±¾Ģāæ¼²éŃõ»Æ»¹Ō·“Ó¦ÓŠ¹Ų¼ĘĖć£¬±Č½Ļ»ł“”£¬×¢ŅāĄūÓĆŹŲŗćĖ¼Ļė½ā“š¼“æÉ£®


 ½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | K+”¢Fe2+”¢Cl-”¢NO${\;}_{3}^{-}$ | B£® | Na+”¢Ba2+”¢Cl-”¢SO${\;}_{4}^{2-}$ | ||
| C£® | NH${\;}_{4}^{+}$”¢Fe3+”¢Cl-”¢SCN- | D£® | K+”¢Mg2+”¢SO${\;}_{4}^{2-}$”¢NO${\;}_{3}^{-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆŗĻ½šÖŠĶÓėĆ¾µÄĪļÖŹµÄĮæÖ®±ČŹĒ1£ŗ2 | |
| B£® | øĆÅØĻõĖįÖŠHNO3µÄĪļÖŹµÄĮæÅØ¶ČŹĒ14.0 mol•L-1 | |
| C£® | NO2ŗĶN2O4µÄ»ģŗĻĘųĢåÖŠ£¬NO2µÄĢå»ż·ÖŹżŹĒ80% | |
| D£® | µĆµ½2.54 g³ĮµķŹ±£¬¼ÓČėNaOHČÜŅŗµÄĢå»żŹĒ640 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 78gNa2O2¹ĢĢåÖŠĖłŗ¬Ąė×Ó×ÜŹżĪŖ4NA | |
| B£® | ³£ĪĀ³£Ń¹ĻĀ£¬14gN2ÓėCO×é³ÉµÄ»ģŗĻĘųĢåŗ¬ÓŠµÄŌ×ÓŹżĪŖNA | |
| C£® | 1molCl2ĶźČ«·“Ó¦Ōņ×ŖŅʵē×ÓŹżŅ»¶ØĪŖ2NA | |
| D£® | Na2O2ÓėĖ®·“Ó¦²śÉś22.4LO2£¬Ōņ×ŖŅʵē×ÓŹżĪŖ2 NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
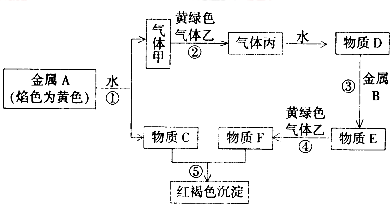
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
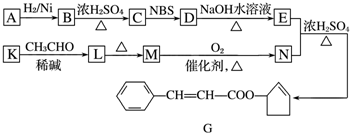
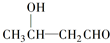
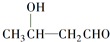 $\stackrel{”÷}{”ś}$CH3CHØTCHCHO+H2O
$\stackrel{”÷}{”ś}$CH3CHØTCHCHO+H2O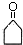 £¬GÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖĢ¼Ģ¼Ė«¼üŗĶõ„»ł£®
£¬GÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖĢ¼Ģ¼Ė«¼üŗĶõ„»ł£® £¬·“Ó¦ĄąŠĶ¼Ó³É·“Ó¦£®
£¬·“Ó¦ĄąŠĶ¼Ó³É·“Ó¦£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ō×ÓŹż | B£® | ·Ö×ÓŹż | C£® | Ģå»ż | D£® | ĪļÖŹµÄĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | SO2£Øg£©+$\frac{1}{2}$O2£Øg£©?SO3£Øg£©”÷H=-98.3 kJ/mol | |
| B£® | 2SO2£Øg£©+O2£Øg£©?SO3£Øl£©”÷H=-196.6 kJ/mol | |
| C£® | SO2£Øg£©+$\frac{1}{2}$O2£Øg£©?SO3£Øg£©”÷H=-122.9 kJ/mol | |
| D£® | 2SO2£Øg£©+O2£Øg£©?SO3£Øg£©”÷H=+196.6 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚŌµē³ŲµÄøŗ¼«ŗĶµē½ā³ŲµÄŅõ¼«ÉĻ¶¼·¢ÉśŹ§µē×ÓµÄŃõ»Æ·“Ó¦ | |
| B£® | ÓƶčŠŌµē¼«µē½āNa2SO4ČÜŅŗ£¬ŅõŃōĮ½¼«²śĪļµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ2 | |
| C£® | ÓƶčŠŌµē¼«µē½ā±„ŗĶNaClČÜŅŗ£¬ČōÓŠ1 molµē×Ó×ŖŅĘ£¬ŌņÉś³É1 mol NaOH | |
| D£® | “ÖĶ¾«Į¶Ź±£¬ÓėµēŌ“Õż¼«ĻąĮ¬µÄŹĒ“æĶ£¬µē¼«·“Ó¦Ź½ĪŖ£ŗCu-2e-=Cu2+ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com