
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
(1)环戊二烯分子中最多有___个原子共平面;
(2)金刚烷的分子式为___________,其分子中的CH2基团有______个;
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:
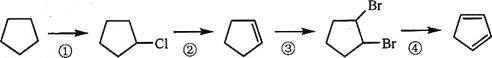
其中,反应①的产物名称是__________,反应②的反应试剂和反应条件是__________,反应③的反应类型是__________;
(4)已知烯烃能发生如下反应:
![]()
请写出下列反应产物的结构简式: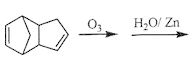 __________;
__________;
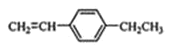
(5)A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(-CH3,-CH2R,-CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基],写出A所有可能的结构简式(不考虑立体异构):_______。
【答案】9 C10H16 6 氯代环戊烷 氢氧化钠醇溶液,加热 加成反应 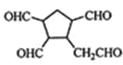
![]() 、
、![]() 、
、![]() 、
、
【解析】
(1)碳碳双键为平面结构,与双键碳直接相连的原子一定在同一平面内;
(2)由结构简式可知,金刚烷的分子中含有6个CH2基团,4个CH基团;
(3)由合成路线可知,反应①为光照条件下,![]() 与氯气发生取代反应生成
与氯气发生取代反应生成 ,反应②为
,反应②为![]() 在氢氧化钠醇溶液中共热发生消去反应生成
在氢氧化钠醇溶液中共热发生消去反应生成![]() ,反应③为
,反应③为![]() 与Br2发生加成反应生成
与Br2发生加成反应生成![]() ;
;
(4)由信息可知,碳碳双键的碳上含H原子被氧化为醛;
(5)A是二聚环戊二烯的同分异构体,则分子式为C10H12,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明含有苯环,苯环的对位位置含有两个取代基,能使溴的四氯化碳溶液褪色,说明分子中含有一个碳碳双键。
(1)碳碳双键为平面结构,与双键碳直接相连的原子一定在同一平面内,环戊二烯分子中含有2个碳碳双键,则5个碳原子可以处于同一平面内,不饱和碳原子上的氢原子也可以处于同一平面内,而饱和碳原子上的2个氢原子不可能处于这个平面上,共有5个C和4个H都有可能在同一平面内,故答案为:9;
(2)由结构简式可知,金刚烷的分子中含有6个CH2基团,4个CH基团,分子式为C10H16,故答案为:C10H16;6;
(3)由合成路线可知,反应①为光照条件下,![]() 与氯气发生取代反应生成
与氯气发生取代反应生成 ,
,![]() 的名称为氯代环戊烷,反应②为
的名称为氯代环戊烷,反应②为![]() 在氢氧化钠醇溶液中共热发生消去反应生成
在氢氧化钠醇溶液中共热发生消去反应生成![]() ,反应③为
,反应③为![]() 与Br2发生加成反应生成
与Br2发生加成反应生成![]() ,故答案为:氯代环戊烷;氢氧化钠醇溶液,加热;加成反应;
,故答案为:氯代环戊烷;氢氧化钠醇溶液,加热;加成反应;
(4)由信息可知,碳碳双键的碳上含H原子被氧化为醛,则![]() 分子中两个碳碳双键断裂生成
分子中两个碳碳双键断裂生成![]() ,故答案为:
,故答案为:![]() ;
;
(5)A是二聚环戊二烯的同分异构体,则分子式为C10H12,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸,说明含有苯环,苯环的对位位置含有两个取代基,能使溴的四氯化碳溶液褪色,说明分子中含有一个碳碳双键,则取代基可能为—CH3和CH2=CHCH2—、CH3CH=CH—、![]() ,可能为—CH2CH3和CH2=CH—,结构简式分别为
,可能为—CH2CH3和CH2=CH—,结构简式分别为![]() 、
、![]() 、
、![]() 、
、 ,故答案为:
,故答案为:![]() 、
、![]() 、
、![]() 、
、 。
。


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:
【题目】25℃时将10mLpH=11的氨水加水稀释至100mL,下列判断正确的是
A.稀释后溶液的pH=7B.氨水的电离度增大,溶液中所有离子的浓度均减小
C.稀释过程中![]() 增大D.pH = 11氨水的浓度为0.001mol/L
增大D.pH = 11氨水的浓度为0.001mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是( )

A. b电极是阴极B. a电极与电源的正极相连
C. 电解过程中水是氧化剂D. b电极附近溶液的pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应①:CO(g)+CuO(s) ![]() CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) ![]() Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g) ![]() CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1=![]()
B.反应③的平衡常数K=![]()
C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应为吸热反应
D.对于反应③,恒温恒容下,增大压强,H2浓度一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种综合处理SO2废气的工艺流程。若每步反应都完全,下列说法正确的是( )
(设反应过程中溶液的体积不变)
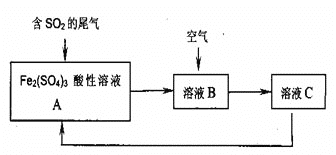
A.溶液B中发生的反应为:2SO2+O2→2SO3
B.由反应过程可推知氧化性:O2>Fe3+>SO42-
C.溶液的pH:A>B>C
D.A与C溶液成分相同,但浓度之比不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列离子在指定溶液中一定能大量共存的是
A.0.1mol·L-1NaHCO3溶液:K+、Al3+、NO3-、SO42-
B.![]() 10-12的溶液中:Na+、K+、ClO-、CO32-
10-12的溶液中:Na+、K+、ClO-、CO32-
C.能使红色石蕊试纸变蓝的溶液:NH4+、K+、Cl-、NO3-
D.水电离的c(H+)=10—11mol·L-1的溶液中:Na+、Ca2+、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取少量溴乙烷的装置如图所示。根据题意完成下列填空:
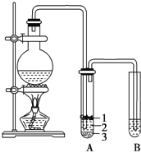
(1)圆底烧瓶中加入的反应物是溴化钠、乙醇 和1:1的硫酸。配制体积比1:1的硫酸所用的仪器为 ________(选填编号)。
a 天平 b 量筒 c 容量瓶 d 烧杯
(2)写出加热时烧瓶中发生的主要反应的化学方程式 ___________________ 。
(3)将 生成物导入盛有冰水混合物的试管A中,冰水混合物的作用是________,试管A中的物质分为三层(如图所示),产物在第____层。
(4)试管A中除了产物和水之外,还可能存在 ________ ,_________ (写出结构简式)。
(5)用浓硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的最佳方法是 ___________(选填编号)。
a 蒸馏 b 氢氧化钠溶液洗涤 c 用四氯化碳萃取 d 用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的物质名称是_________。
(6)实验员老师建议把上述装置中的仪器连接部分由橡胶管改成标准玻璃接口,其原因_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500℃时,在四个体积为2L的恒容密闭容器中发生反应:NO2(g) + SO2(g)![]() SO3(g)+ NO(g)。有关物质起始时的物质的量数据如下表所示:
SO3(g)+ NO(g)。有关物质起始时的物质的量数据如下表所示:
容器 | 起始时物质的量/mol | |||
NO2 | SO2 | SO3 | NO | |
甲 | 0.1 | 0.1 | 0 | 0 |
乙 | 0.15 | 0.05 | 0.05 | 0.05 |
丙 | 0 | 0 | 0.2 | 0.2 |
丁 | 0.1 | 0.2 | 0 | 0 |
已知甲容器达到平衡时容器中c(SO3)=0.01mol·L-1。下列说法正确的是
A.升温至700℃,上述反应的平衡常数为![]() ,则正反应为吸热反应
,则正反应为吸热反应
B.达平衡时,容器丙中c(SO2)是容器甲的2倍
C.达平衡时,容器丁中c(NO)与乙容器中相同
D.保持温度不变容器甲达到平衡时再充入SO2(g)和SO3(g)各0.02mol,此时v(正)>v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 均是短周期元素,它们在元素周期表中的相对位置如图所示,其中
均是短周期元素,它们在元素周期表中的相对位置如图所示,其中![]() 与
与![]() 形成的一种化合物能使品红溶液褪色,下列说法正确的是( )
形成的一种化合物能使品红溶液褪色,下列说法正确的是( )

A.![]() 与
与![]() 形成的两种常见化合物中含有的化学键类型全部相同
形成的两种常见化合物中含有的化学键类型全部相同
B.可用![]() 溶液除去
溶液除去![]() 单质中混有的
单质中混有的![]() 单质
单质
C.简单氢化物的热稳定性:![]()
D.化合物![]() 和
和![]() 中,阳离子半径均大于阴离子半径
中,阳离子半径均大于阴离子半径
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com