
 �����£���0��l mol��L-lNa2A��Һ�У�����ͨ��HC1��H2A��HA-��A2-����Һ����ռ���ʵ����������ģ���pOH[pOH=-lgc��OH-��]�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
�����£���0��l mol��L-lNa2A��Һ�У�����ͨ��HC1��H2A��HA-��A2-����Һ����ռ���ʵ����������ģ���pOH[pOH=-lgc��OH-��]�Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | H2A�ĵڶ�������ƽ�ⳣ��Ϊl0-l0mol/L | |
| B�� | ����HCl��ͨ�룬$\frac{c��{H}^{+}��}{c��{H}_{2}A��}$�ȼ�С������ | |
| C�� | ����Һ������ʱ��c��Na+���Tc��HA-��+2c ��A2-�� | |
| D�� | ����Ũ�ȵ������Na2A��H2A��Һ��Ϻ���Һ�Լ��� |
���� pOHΪOH-���ӵĸ�������pOHԽ����OH-Ũ��ԽС����Һ����Խǿ����ͼ���֪����0��l mol��L-lNa2A��Һ�У�����ͨ��HC1��A2-��С������HA-��HA-Ũ���������С����������H2A����pOH=10ʱ��HA-��A2-Ũ����ȣ��Դ˽����⣮
��� �⣺A����pOH=10ʱ��c��H+��=l0-4mol/L��HA-��A2-Ũ����ȣ�H2A�ĵڶ�������ƽ�ⳣ��Ϊ$\frac{c��{A}^{-}��c��{H}^{+}��}{c��H{A}^{-}��}$=l0-4mol/L����A����
B���¶Ȳ��䣬��H2A�ĵ�һ�������ƻ��������䣬��$\frac{c��H{A}^{-}��c��{H}^{+}��}{c��{H}_{2}A��}$���䣬����HA-Ũ���������С����$\frac{c��{H}^{+}��}{c��{H}_{2}A��}$�ȼ�С������B��ȷ��
C������Һ������ʱ��c��Na+���Tc��HA-��+2c ��A2-��+c��Cl-������C����
D������Ũ�ȵ������Na2A��H2A��Һ��Ϻ�Ӧ����NaHA����A��֪H2A�ĵڶ�������ƽ�ⳣ��Ϊ$\frac{c��{A}^{-}��c��{H}^{+}��}{c��H{A}^{-}��}$=l0-4mol/L����HA-��ˮ�ⳣ��Ϊ$\frac{Kw}{Ka}$=l0-l0����֪HA-�������ˮ��̶ȣ���Һ�����ԣ���D����
��ѡB��
���� �����ۺϿ�������ϵĶ����жϺͼ��㣬Ϊ��Ƶ���㣬���ؿ���ѧ���ķ��������ͼ�������������ע����յ��롢ˮ�ⳣ���ļ����Ӧ�ã�����ʱע����ᣬ�Ѷ��еȣ�


 С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д� ��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д�
��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ��Ŀ�� | ʵ�鷽�� | ��ѡ�������� | |
| A | ��ȥKNO3������NaC1 | ��������Ƴ��ȵı�����Һ����ȴ�ᾧ������ | �ƾ��ơ��ձ��������� |
| B | ֤��HClO ��CH3COOH������ǿ�� | ͬ���£���pH��ֽ��Ũ�Ⱦ�Ϊ0.1mol•L-1��NaClO��Һ��CH3COONa��Һ��pH | ������������Ƭ |
| C | ��������ˮ�������л�ԭ�� | ��������Һ��ˮ���뼸��ϡ���ᣬˮԡ���ȼ����ӣ��������м������Ƶ�������Һ����ˮԡ���� | �Թܡ��ձ����ƾ��ơ��ι� |
| D | ����1L1.6%��CuSO4��Һ����Һ�ܶȽ���Ϊ1g/mL�� | ��25g CuSO4•5H2O�ܽ���975gˮ�� | �ձ�������������ͷ�ιܡ���Ͳ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Na[Al��OH��4]��Һ��ͨ������CO2��2[Al��OH��4]-+CO2�T2Al��OH��3��+CO32-+H2O | |
| B�� | �������������������Һ��Ӧ��SiO2+2Na++2OH-�TNa2SiO3+H2O | |
| C�� | ͭ���Ȼ�����Һ��Ӧ��2Fe3++Cu�T2Fe2++Cu2+ | |
| D�� | ̼�ᱵ��ϡ���ᷴӦ��CO32-+2H+�TCO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ����5�ֹ����� | |
| B�� | ����ʽΪC9H9O6 | |
| C�� | ���Է���ȡ�����ӳɡ���ȥ��������Ӧ | |
| D�� | �˴Ź���������6���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3COOH��C2H518OH��Ũ���������¼��ȣ���Ӧ���ɵ��л�����ӵĽṹ��ʽΪCH3COOC2H5 | |
| B�� | �����ñ���̼������Һ�����Ҵ������ᡢ�������Ȼ�̼ | |
| C�� | �л���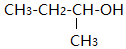 ������Ϊ1-��-1-���� ������Ϊ1-��-1-���� | |
| D�� | �������Һ�м�������ϡ�������м����ӣ���ȴ�����������Һ��ˮԡ����һ��ʱ��û������������˵��������δˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 14g ����ʽΪCnH2n�������к��е�C-H������ĿΪ2NA | |
| B�� | Na2O2��H2O�ķ�Ӧ��ÿ����0.1molO2��ת�Ƶ�����ĿΪ0.4NA | |
| C�� | ���³�ѹ�£�1.7g NH3����������Ϊ0.8NA | |
| D�� | ��״���£�11.2L NO��11.2LO2��ϣ�ԭ������С��2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 12.0gNaHSO4��������������Ϊ0.2NA�� | |
| B�� | 0.1 mol Cu�������ȵ�Ũ���ᷴӦ����SO2�����ԼΪ22.4 L | |
| C�� | T��ʱ��1L pH=6�Ĵ�ˮ�У���1��10-6NA��H+ | |
| D�� | ��״���£�1 L pH=13��NaOH��Һ��OH-Ϊ0.1NA�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com