
【题目】A是单质,D是A单质所含元素的最高价氧化物的水化物,甲、乙、丙、丁四种化合物间除甲与丁、丙与乙外,两两均能发生中和反应。已知有如下转化关系(部分产物和反应条件已略去):

试回答:
(l)写出B在工业生产中的一种用途:__________________,用化学方程式表示A物质在工业生产中的一种用途:__________________。
(2)写出B转化为C的可能的离子方程式____________;_____________。
(3)若C的溶液显酸性,用离子方程式表示其净水的原理___________________。
(4)若C为钠盐,用含m mol C的溶液与1Lnmol/L的盐酸充分反应,已知m/n=1/2,则生成D的物质的量为__________mol。
【答案】(1)工业上制备Al(或作耐火材料)2Al+Fe3O2=2AlO2-+ 2Fe
(2)Al2O3+6H+=2Al3++3H2O、Al2O3+2OH-=2AlO2-+H2O
(3)Al3++3H2O![]() Al(OH)3(胶体)+3H+ (4)
Al(OH)3(胶体)+3H+ (4)![]() (或
(或![]() ,或
,或![]() )
)
【解析】
试题分析:A是单质,与氧气反应生成B为氧化物,甲、乙、丙、丁四种化合物间除甲与丁、丙与乙外,两两均能发生中和反应,为酸与碱的反应,甲与丁为同类物质,丙与乙为同类物质,氧化物B能与酸或碱反应生成C,D是A单质所含元素的最高价氧化物的水化物,结合转化关系,可推知B为Al2O3,则A为Al、C为Al(OH)3,则:
(1)Al2O3在工业上制备Al(或作耐火材料);
(2)B转化生成C为氧化铝与强碱或强酸的反应,反应离子方程式为:Al2O3+6H+=2Al3++3H2O 或Al2O3+2OH-=2AlO2-+H2O;
(3)若C的溶液显酸性,则C为铝盐,溶液中铝离子水解Al3++3H2O![]() Al(OH)3(胶体)+3H+,生成氢氧化铝胶体,可以净水;
Al(OH)3(胶体)+3H+,生成氢氧化铝胶体,可以净水;
(4)若C为钠盐,则甲为NaOH,C为NaAlO2,1L n molL-1的盐酸中n(HCl)=n mol,由于n(NaAlO2):n(HCl)=1:2,故按AlO2-+H2O+H+=Al(OH)3↓反应,盐酸有剩余,能部分溶解氢氧化铝,则:
AlO2-+H2O+H+=Al(OH)3↓
m mol m mol m mol
剩余n(H+)=n mol-m mol=(n-m)mol
Al(OH)3+3H+=Al3++3H2O
(nm) /3 mol (n-m)mol
故得到氢氧化铝沉淀为![]() mol。
mol。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列化合物的用途叙述正确的是
A.光纤通信使用的光缆的主要成分是晶体Si,太阳能电池使用的材枓主要娃SiO2
B.水玻璃可用作防火剂或防腐剂
C.高锰酸钾溶液、酒精、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性
D.SO2可用来漂白纸浆、毛、丝、草帽辫、增白食品等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为值。下列说法正确的是
A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
C.常温常压下,Na2O2与足量H2O反应,共生成0.2 mol O2,转移电子的数目为0.8NA
D.标准状况下,2.24 L已烷含有分子的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.二氧化硫可以使溴水褪色是因为它有漂白性
B.浓硫酸可用于干燥H2S和CO2
C.可以用加热法除去NaCl固体中的混有的NH4Cl
D.过量的Cu与浓硝酸反应不可能有一氧化氮生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验装置如下图所示。先关闭K,使A中的反应进行,加热玻璃管C,可观察到C管中发出耀眼白光,产生白烟,管壁上附着有淡黄色物质。实验完成后,将C管中固体全部加入盐酸中,有臭鸡蛋气味的气体生成。请回答下列有关问题:
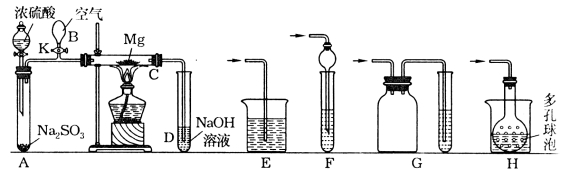
(1)C中全部产物有 、 、 。
(2)本实验先使A中反应进行,再加热C装置,其目的是 。
(3)停止实验时,先打开K,再停止滴加浓硫酸,熄灭酒精灯,橡胶气胆B在实验中的作用是 。
(4)若无装置B、K,使用普通导管,本实验的尾气吸收装置可以选用上图中装置 (填写序号,多选扣分)。
(5)C中的Mg应放在不锈钢垫片上而不能直接接触管壁的原因是
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。下图是工业上用印刷电路的蚀刻液的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:

按要求回答下列问题:
⑴ 废液①的主要含有的金属阳离子是__________(填化学符号,下同);废渣①的成分是_____________,Y为__________。
⑵废液①与Z反应的离子方程式为:______________________。
⑶ 写出废渣②生成二氧化硫的化学方程式_____________________。
⑷ 为得到纯净的CuCl晶体,可用下列_________(填序号)进行洗涤。
a.纯净水 b.乙醇 c.稀硫酸 d.氯化铜溶液
⑸ 生产过程中调节溶液的pH不能过大的原因是___________________。
⑹ 写出产生CuCl的离子方程式_______________________。
⑺ 氯化亚铜的定量分析:
① 称取样品0.25g加入10mL过量的FeCl3溶液250mlL锥形瓶中,不断摇动;
② 待样品溶解后,加水50mL和2滴指示剂;
③ 立即用0.10 mol·L-1硫酸铈标准溶液滴至绿色出现为终点;
④ 重复三次,消耗硫酸铈溶液平均体积为25.00mL。
已知:CuCl的分子式量为99;CuCl + FeCl3 = CuCl2 + FeCl2; Fe2+ + Ce4+ = Fe3+ + Ce3+。
则CuCl的纯度为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 Mg、Al、Fe、Cu都是重要的金属元素。下列说法正确的是( )
A.四者对应的氧化物均为碱性氧化物
B.四者的单质放置在空气中均只生成氧化物
C.常温下,Al、Fe不与浓硝酸反应,而Cu能与浓硝酸、稀硝酸反应
D.Fe分别与氯气和稀盐酸反应所得氯化物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.医用酒精是质量分数为95%的乙醇溶液
B.用过滤的方法可以分离乙酸乙酯和乙酸
C.葡萄糖、氨基酸在一定条件下都能发生酯化反应
D.往蛋白质溶液中加入浓的CuSO4溶液,蛋白质会发生盐析
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com