
| A. | SO42-的空间构型是正四面体形 | |
| B. | CS2分子中各原子均达8电子稳定结构 | |
| C. | 甲醛分子中碳原子的杂化类型为sp2 | |
| D. | CO2与SO2为等电子体 |
分析 A.SO42-中价层电子对个数是4且不含孤电子对,空间构型是正四面体形;
B.ABn型分子,A的族序数+成键数=8,则满足所有原子均达到8e-稳定结构;
C.根据价层电子对互斥理论确定原子杂化类型,中心原子价层电子对个数是3,据此判断C原子杂化类型;
D.原子总数相同、电子总数或价电子总数相同的互为等电子体.
解答 解:A.根据价层电子对互斥理论,价层电子对个数=σ键+孤电子对个数,SO42-中中心原子S的价层电子对为$\frac{6+2}{2}$=4,孤电子对数为$\frac{6+2-2×4}{2}$=0,不含孤电子对,所以空间构型是正四面体结构,故A正确;
B.CS2中族序数+成键数=4+4=8,分子中各原子均达到8e-稳定结构,故B正确;
C.甲醛分子中含有碳氧双键,1个甲醛分子中含有2个碳氢σ键,1个碳氧σ键,共有3个σ键,则碳原子轨道的杂化类型为sp2杂化,因此甲醛中碳原子采取sp2杂化,故C正确;
D.CO2与SO2分子中原子个数相等,电子总数分别为22、32,价电子总数分别为16、18,都不相同,所以不是等电子体,故D错误;
故选D.
点评 本题考查较综合,涉及原子杂化方式的判断、空间构型、等电子体等,为高考频点,明确等电子体的概念以及根据价层电子对互斥理论来分析是解答关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 等量的硫蒸气和硫固体分别完全燃烧,前者放出热量少 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热量大于57.3kJ | |
| C. | 由C(石墨,s)→C(金刚石,s)△H=+1.5kJ/mol可知,金刚石比石墨稳定 | |
| D. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=+285.8kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,3,5,5-四甲基-4,4-二乙基己烷是一个正确的系统命名 | |
| B. | 等质量的乙炔与苯完全燃烧所消耗的氧气的质量相同,生成的CO2的量不同 | |
| C. | 丙烯醛(CH2═CHCHO)在一定条件下与H2充分反应生成1-丙醇 | |
| D. | 乙酸的某种同系物Q存在同类物质的同分异构体,则Q的分子式可能为C3H6O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O的反应中,生成28 g N2,转移的电子数目为3.75NA | |
| B. | 室温下,1 L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 标准状况下,2.24L SO3中所含原子数为0.4 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸雨是指PH<7的雨水,酸雨长时间放置,酸性变强 | |
| B. | 用排空气法收集NO | |
| C. | 用加热浓氨水的方法可以快速制氨气,经氯化钙干燥后得到纯净的氨气 | |
| D. | 2NH3+Cl2=6HCl+N2,因此可以用浓氨水检验氯气的管道是否漏气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
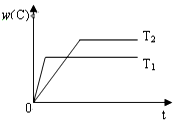 对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )
对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )| A. | T1>T2,正反应放热 | B. | T1<T2,正反应放热 | ||
| C. | T1>T2,正反应吸热 | D. | T1<T2,正反应吸热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 46gNO2和N2O4混合气体中含有原子总数为3NA | |
| B. | 1.7gH2O2中含有的电子数为0.8NA | |
| C. | 标准状况下,2.24L戊烷所含分子数为0.1NA | |
| D. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,钠失去2NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热,观察是否有气体放出 | |
| B. | 取少量固体配成稀溶液,滴加石灰水,观察有无沉淀生成 | |
| C. | 取少量固体配成稀溶液,滴加氯化钡溶液,观察有无沉淀生成 | |
| D. | 加热前后称量固体,比较固体质量是否变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com