
| A�� | ֻ�Тڢ� | B�� | ֻ�Тۢ� | C�� | ֻ�Т� | D�� | �٢ڢۢ� |
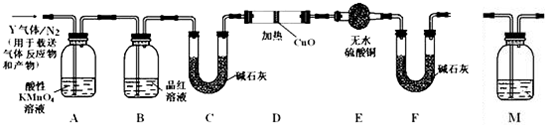
���� ��ַ�Ӧ��Ϊ�˼�������ͭ�Ƿ���ȫ��Ӧ����������CuO��Ӧ��������ͭ��Һ������ͭ��Fe�����û���Ӧ���Դ������
��� �⣺�ټ���ϡ���������ݲ�����˵��Alʣ�࣬��CuO��ȫ��Ӧ���ʲ�ѡ��
�ڼ���ϡ�����û���������ɣ�����˵��������Al��CuOǡ����ȫ��Ӧ���ʲ�ѡ��
�ۼ���ϡ�������Һ���к�ɫ��������֣�ֻ��˵����Cu���ɣ�����˵��CuO�Ƿ���ȫ��Ӧ���ʲ�ѡ��
�ܲ�����Һ����Ƭ�����к�ɫ������������CuOʣ�࣬��˵������ͭû����ȫ��Ӧ����ѡ��
��ѡC��
���� ���⿼�����ʵļ���ͼ��飬Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ������Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| �� | ��ˮ�����c��H+��=l��l0-14mol/L����Һ�У�Ca2+��K+��Cl-��HCO3- | |
| �� | ��ʹpH��ֽ�ʺ�ɫ����Һ��Na+��NH4+��I-��NO3- | |
| �� | Kw/c��H+��=0.1mol/L����Һ��Na+��K+��SiO32-��NO3- | |
| �� | FeCl2��Һ��K+��Na+��SO42-��AlO2- |
| A�� | �� | B�� | �� | C�� | �� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 A��B��C��D����Ԫ�صĺ˵������С��18��AԪ��ԭ�Ӻ���ֻ��1�����ӣ�B�ǵؿ��к�������Ԫ�أ�B��C���γ����ֻ�����CB��CB2��C���������������۾���ֵ��ȣ�CB�ж���CB2���������D+������Neԭ����ͬ�ĵ��Ӳ�ṹ��
A��B��C��D����Ԫ�صĺ˵������С��18��AԪ��ԭ�Ӻ���ֻ��1�����ӣ�B�ǵؿ��к�������Ԫ�أ�B��C���γ����ֻ�����CB��CB2��C���������������۾���ֵ��ȣ�CB�ж���CB2���������D+������Neԭ����ͬ�ĵ��Ӳ�ṹ�� ��CB2�ĵ���ʽΪ
��CB2�ĵ���ʽΪ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol H2������ֻ���ڱ�״���²�ԼΪ2g | |
| B�� | �ڱ�״����ij����������22.4L������Ϊ����������ʵ���Լ��1mol | |
| C�� | ��20��ʱ��1mol�κ����������ܱ�22.4L�� | |
| D�� | 1mol H2��O2�Ļ���������������Ϊ34g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����ᣨ��ͼ����������������ҩ����Ұ���ܲ�����Ҷˮ�ա�������У���������ֹѪ���ã����� ���ڿ������˵������ȷ���ǣ�������
�����ᣨ��ͼ����������������ҩ����Ұ���ܲ�����Ҷˮ�ա�������У���������ֹѪ���ã����� ���ڿ������˵������ȷ���ǣ�������| A�� | ������ķ���ʽΪC9H8O4 | |
| B�� | 1 mol��������Ժͺ�4 molBr2��Ũ��ˮ��Ӧ | |
| C�� | 1 mol������������NaHCO3��Һ��Ӧ�ܲ��������Լ67.2L��CO2 | |
| D�� | �������ø�����ؼ��鿧��������е�̼̼˫�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com