
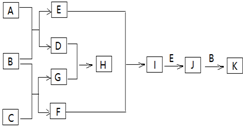
 有关物质的转化关系如图所示(部分物质与条件已略去).已知A为淡黄色固体,B为常见的无色液体,C为两种元素组成的化合物,摩尔质量为150g/mol,E为单质气体,F为气态氢化物,有臭鸡蛋气味,G为两性氢氧化物,K为常见的酸.
有关物质的转化关系如图所示(部分物质与条件已略去).已知A为淡黄色固体,B为常见的无色液体,C为两种元素组成的化合物,摩尔质量为150g/mol,E为单质气体,F为气态氢化物,有臭鸡蛋气味,G为两性氢氧化物,K为常见的酸. .
.分析 A为淡黄色固体,B为常见的无色液体,二者反应生成D与气体单质E,则A为Na2O2,B为H2O,E为O2,D为NaOH,两种元素组成的化合物C能与水反应得到两性氢氧化物G与臭鸡蛋气体的气体F,G为Al(OH)3,F为H2S,C含有Al、S两种元素,其摩尔质量为150g/mol,则C为Al2S3,K为常见的酸,由转化关系可知,H为NaAlO2,I为SO2,J为SO3,K为H2SO4.
解答 解:A为淡黄色固体,B为常见的无色液体,二者反应生成D与气体单质E,则A为Na2O2,B为H2O,E为O2,D为NaOH,两种元素组成的化合物C能与水反应得到两性氢氧化物G与臭鸡蛋气体的气体F,G为Al(OH)3,F为H2S,C含有Al、S两种元素,其摩尔质量为150g/mol,则C为Al2S3,K为常见的酸,由转化关系可知,H为NaAlO2,I为SO2,J为SO3,K为H2SO4.
(1)C的化学式为:Al2S3,故答案为:Al2S3;
(2)B的电子式为: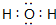 ,故答案为:
,故答案为: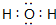 ;
;
(3)反应A+B→D+E的化学方程式:2Na2O2+2H2O=4NaOH+O2↑,故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(4)反应D+G→H的离子方程式:Al(OH)3+OH-=AlO2-+2H2O,故答案为:Al(OH)3+OH-=AlO2-+2H2O.
点评 本题考查无机物推断,涉及硫酸工业以及Al、S元素化合物性质等,“淡黄色固体A与无色液体B反应得到气体单质E”是推断突破口,结合元素化合物性质进行土地,需要学生熟练掌握元素化合物知识,难度中等


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 用10mL量筒量取8.10mL稀盐酸 | |
| B. | 用pH计测得某溶液的pH为2.3 | |
| C. | 用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸 | |
| D. | 可用50.00mL碱式滴定管量取20.00mL KMnO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
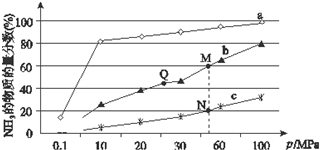 合成氨反应是化学上最重要的反应之一:
合成氨反应是化学上最重要的反应之一:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用明矾可以对水进行消毒、杀菌 | |
| B. | 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 | |
| C. | 浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果 | |
| D. | 信息产业中的光缆的主要成分是单质硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com