


 Сѧ������ҵϵ�д�
Сѧ������ҵϵ�д� ��ʿһ��ȫͨϵ�д�
��ʿһ��ȫͨϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1��0.1mol/LNa2CO3��Һ��
��1��0.1mol/LNa2CO3��Һ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
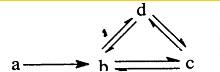
| A��Na Na2O2 NaOH Na2CO3 | B��S SO2 H2SO3 NaHSO3 | C��Cu CuO Cu��OH��2 CuSO4 | D��Si SiO2 H2SiO3 Na2SiO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ�꼪��ʡ��У����������ڶ������������ۻ�ѧ�Ծ��������棩 ���ͣ������
��1�����ɽ���Ԫ�������γɶ��������磺[Fe(H2NCONH2)6] (NO3)3[�����������غ���(��)]��Fe(CO)x�ȡ�
�� ��̬Fe3+��M������Ų�ʽΪ ��
�� ����(H2NCONH2)������C��Nԭ�ӵ��ӻ���ʽ�ֱ��� �� ��
�� �����Fe(CO)x������ԭ�Ӽ۵������������ṩ������֮��Ϊ18����x= �� Fe(CO)x�����³�Һ̬���۵�Ϊ��20.5�棬�е�Ϊ103�棬�����ڷǼ����ܼ����ݴ˿��ж�Fe(CO)x�������� ��������ͣ�

��2��O��Na�γɵ�һ��ֻ�������Ӽ������ӻ�����ľ����ṹ����ͼ����һ����������Χ���������������Ϊ���㹹�ɵļ�����Ϊ ����֪�þ������ܶ�Ϊ�� g/cm3�������ӵ�����ΪNA�����߳�a= cm�� (�ú��ѡ�NA�ļ���ʽ��ʾ)
��3������˵����ȷ���� _��
A����һ�����ܴ�С��S��P��Si
B���縺��˳��C��N��O��F
C����Ϊ������CaO��KCl�ߣ�����KCl��CaO�۵��
D��SO2��CO2�Ļ�ѧ�������ƣ����ӽṹҲ����ֱ���ͣ���ͬ������SO2���ܽ�ȸ���
E�����Ӿ����У����ۼ�����Խ�÷��Ӿ�����۷е�Խ��
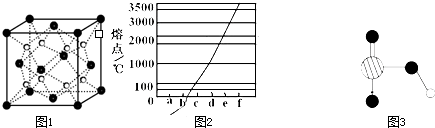
��4��ͼ1��Na��Cu��Si��H��C��N��Ԫ�ص��ʵ��۵�ߵ͵�˳������c��d�����Ⱥ͵�������塣

�� ͼ��d���ʵľ���ѻ���ʽ������ ��
�� ����a��b��f ��Ӧ��Ԫ����ԭ�Ӹ�����1:1:1�γɵķ����к� ���Ҽ��� ���м���
�� ͼ2����������Ԫ���е�һ��Ԫ���γɵĺ�����Ľṹ�����Ҫ˵��������������ˮ��ԭ�� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com