

|
|
| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |


科目:高中化学 来源: 题型:
| A、原氨水物质的量浓度为0.1 mol?L-1 |
| B、反应后的溶液中c(NH4+)+c(NH3?H2O)+c(NH3)=0.1 mol?L-1 |
| C、反应后的溶液中:c(Clˉ)>c(NH4+)>c(H+)>c(OHˉ) |
| D、原氨水中:c(NH4+)+c(H+)=c(OHˉ) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、苯酚钠溶液中通入二氧化碳:2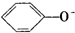 +CO2+H2O→CO32-+2 +CO2+H2O→CO32-+2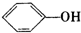 |
| B、醋酸溶液中加入氢氧化钠溶液:H++OH-═H2O |
| C、向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-═Mg(OH)2↓+2CO32-+2H2O |
| D、碳酸氢钠溶液呈碱性:HCO3-+H2O?CO32-+H3O+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、3.2 g O2与O3的混合物中含有的氧原子数为0.2NA |
| B、标准状况下,11.2 L乙醇中含有的碳氢键数为2.5NA |
| C、标准状况下,30gNO和16gO2混合所生成的气体分子数为NA |
| D、标准状况下电解硫酸铜溶液时,阳极每生成气体3.36 L,转移电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe2+、K+、SO42─、Cl─ |
| B、Ca2+、Mg2+、HCO3─、NO3─ |
| C、Al3+、Na+、SO42─、NO3─ |
| D、K+、Na+、SiO32─、AlO2─ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16g02和O3的混合气体所含氧原子数在NA/3到NA/2之间 |
| B、62g Na2O与78gNa202含有的离子数均为3NA |
| C、1molC5H12含共价键数为20NA |
| D、1LO.lmol/L的醋酸溶液中所含离子总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴人甲基橙显红色的溶液中:NH4+、Ba2+、AlO-2、Cl- | ||||
B、Kw/c(H+)=0.1 mol/L的溶液:Na+、K+、Si
| ||||
C、含有较多S
| ||||
D、澄清透明溶液中:K+、Mn
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=0的溶液中:Fe3+、Mg2+、Cl-、SO42- |
| B、水电离出的c(H+)=1×10-13mol/L的溶液中:K+、HCO3-、Cl-、S2- |
| C、使紫色石蕊试液显蓝色的溶液中:Mg2+、NO3-、Fe3+、SO42- |
| D、溶有碳酸氢钠的溶液:K+、SO42-、Cl-、OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com