
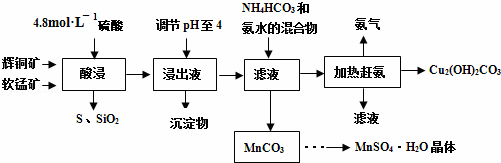
���� ���̷�����֪��ͭ�����̿��������������˵õ�����Һ������ҺPH��ʹ������ȫ�����������˵õ�����Һ����Ҫ����CuSO4��MnSO4�ȣ�����̼����狀Ͱ�ˮ���˵õ������Һ���ȸϳ������ᾧ�����õ���ʽ̼��ͭ������Ϊ̼���̣�ͨ������Ũ������ȴ�ᾧ����ϴ�ӵõ������̾��壻
��1������250mL��Һ����Ҫ250mL����ƿ������Ҫ��ͷ�ιܶ��ݣ�
��2����ʯ�Ŀ�����С���¶ȼ��Ƿ����Ȼ�Ӱ���ȡ�ʣ�
��3��MnO2�н�ǿ�������ԣ��ܽ����������е�������Ϊ��������������CuSO4��MnSO4��S����Ӧ�������ᡢ�������̺�����ͭ�����ݻ��ϼ���������ƽ��
��4������������ʼ����PH=1.5����ȫ����PH=3.2��Cu2+����ʼ������4.4��ʹFe3+��ȫ������Cu2+��������PH��Χ�ǣ�3.2��4.4��
��5�����ݹ������̿��Կ�������ѭ��ʹ�õ������ǰ�����
��6��MnSO4•H2O�����ھƾ����ܽ��С��
��7�����ݵζ���Ӧ���ɵij���Ϊ���ᱵ�����Ԫ���غ����õ���Ʒ���ȣ�
��� �⣺��������У��������費��Ӧ�����������Cu2S��Ӧ����S���ʣ�Fe2O3�ܽ����Һ��pHֵ������4ʱ��Fe3+���������˵õ�����Һ�ɷ�ӦΪCuSO4��MnSO4�ȣ����ȸ�����õ���ʽ̼��ͭ������Ϊ̼���̣�ͨ������Ũ������ȴ�ᾧ������ϴ�ӵȲ������ɵõ������̾��壬
��1������һ�����ʵ���Ũ�ȵ���Һ���ز����ٵ�������ƿ�ͽ�ͷ�ιܣ�����ƿҪ������������ʹ��250mL����ƿ��
�ʴ�Ϊ��250mL����ƿ����ͷ�ιܣ�
��2���������ʱ��ʯ������СӰ���ȡ�ʣ�����ͨ�������ʯ��߽�ȡ�ʣ��������ʵ������¶Ȼ��߽�����߽�ȡ�ʣ�
�ʴ�Ϊ�������ʯ���ʵ������¶Ȼ��߽��裻
��3��������Ϣ��MnO2�ܽ����������е�������Ϊ������Ӧ����Cu2S��MnO2��H2SO4 ����������CuSO4��MnSO4��S��������ͭ�������壬���ϼ۱仯�ǣ���1��2+2��1��=4��MnԪ�ػ��ϼ۱仯�ǣ�4-2=2�����Զ������̻�ѧ��������2������ͭ����1���ٸ��ݹ۲취��ƽ�������ʣ���Ӧ�Ļ�ѧ����ʽ�ǣ�Cu2S+2MnO2+4H2SO4=2CuSO4+2 MnSO4+S��+4H2O��
�ʴ�Ϊ��Cu2S+2MnO2+4H2SO4=2CuSO4+2 MnSO4+S��+4H2O��
��4�����ݽ��������������������������pH��Χ��ʹFe3+��ȫ������Cu2+��������PH��Χ�ǣ�3.2��4.4����ѡ��PH=4Ŀ����ʹFe3+��ȫˮ��������������������
�ʴ�Ϊ��ʹFe3+��ȫˮ��������������������
��5�����������У������˰�ˮ������ֵõ��˰�����NH3 ��ѭ��ʹ�ã�
�ʴ�Ϊ��NH3��
��6����õ�MnSO4•H2O������Ҫ��һ��ϴ�ӡ����ϴ��ʱӦ�þƾ����ھƾ��У������̾����ܽ��С���ʻ�õ�MnSO4•H2O������þƾ�ϴ�ӣ�Ŀ���Ǽ���MnSO4•H2O�������ʧ��
�ʴ�Ϊ���ƾ���
��7���ⶨMnSO4•H2O��Ʒ�Ĵ��ȣ�ȷ��ȡ��Ʒ14.00g��������ˮ���100mL��Һ��ȡ��25.00mL�ñ���BaCl2��Һ�ⶨ����ȫ��Ӧ��õ���4.66g����Ϊ���ᱵ�������ʵ���Ϊ��n��BaSO4��=n��SO42-��=n��MnSO4•H2O��=$\frac{4.66}{233}$mol=0.02mol�������Ʒ��MnSO4•H2O���ʵ���Ϊ��0.02mol��$\frac{100}{25}$=0.08mol������Ʒ��MnSO4•H2O�Ĵ���=$\frac{0.08mol��169g/mol}{14.00g}$��100%=96.57%��
�ʴ�Ϊ��96.57%��
���� ���⿼�����Ʊ���������ƣ���Ŀ�Ѷ��еȣ����ݹ���������ȷʵ��ԭ��Ϊ���ؼ�������֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ�����ѧ���ķ�����������������ѧʵ��������


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
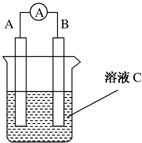 ��ͼ��ʾ��ԭ��ص�װ��ͼ��
��ͼ��ʾ��ԭ��ص�װ��ͼ�� Ϊ������������ش�
Ϊ������������ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| װ�� | 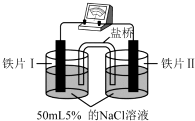 | 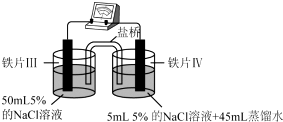 |
| ���� | ������ָ��δ����ƫת | ������ָ��ƫת |
| A�� | ��������ָ��δ����ƫת����˵����Ƭ����Ƭ���δ����ʴ | |
| B�� | ��K3[Fe��CN��6]��Һ������Ƭ��������Һ�����жϵ�ص��������� | |
| C�� | ��Ƭ�������ĵ������ҺŨ����ͬ�����ߵĸ�ʴ������� | |
| D�� | ��Ƭ���ĵ缫��ӦʽΪFe-3e-=Fe3+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
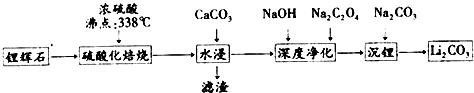
| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
| Li2CO3 | 1.54 | 1.43 | 1.33 | 1.25 | 1.17 | 1.08 | 1.01 | 0.85 | 0.72 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij������ɫ��Ӧ�ʻ�ɫ���������к���K+ | |
| B�� | �㷺pH��ֽ���ij������Һ��pHΪ12.5 | |
| C�� | ����ƿ���������ܽ����ʵ����� | |
| D�� | ���ε��ᴿ�����У���Һ�������м��������ᾧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com