
Ⅰ.选择下列实验方法分离物质,将分离方法的序号填在横线上。
A、萃取分液法 B、渗析 C、结晶法 D、分液法 E、蒸馏法 F、过滤法
(1)分离饱和食盐水和沙子的混合物
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾
(3)分离水和苯的混合物
 (4)分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),已知四氯化碳和甲苯互溶 。
(4)分离四氯化碳(沸点为76.75°C)和甲苯(沸点为110.6°C),已知四氯化碳和甲苯互溶 。
Ⅱ.(1)指出右图装置中A、B的名称
A B
(2)分液操作中用到的主要仪器是 。
科目:高中化学 来源: 题型:
工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
下列叙述正确的是( )
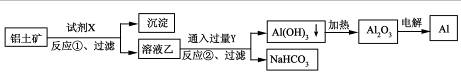
A.试剂X可以是氢氧化钠溶液,也可以是盐酸
B.反应①、过滤后所得沉淀为氢氧化铁
C.图中所示转化反应都不是氧化还原反应
D.反应②的化学方程式为NaAlO2 + CO2 + 2H2O=Al(OH)3↓ + NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年10月9日,2013年诺贝尔化学奖在瑞典揭晓,犹太裔美国理论化学家马丁·卡普拉斯、 美国斯坦福大学生物物理学家迈克尔·莱维特和南加州大学化学家亚利耶·瓦谢尔因给复杂化学体系设计了多尺度模型而分享奖项。三位科学家的研究成果已经应用于废气净化及植物的光合作用的研究中,并可用于优化汽车催化剂、药物和太阳能电池的设计。
汽车尾气净化的主要原理为:2NO(g) + 2CO(g) 2CO2(g)+ N2(g) △H<0
2CO2(g)+ N2(g) △H<0
(1)同一条件下该反应正反应的平衡常数为K1,逆反应的表达式平衡常数为K2,K1与K2的关系式为 ▲ 。
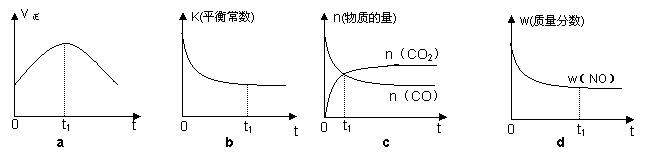
(2)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 ▲ (填代号)。

(3)在体积为10L的密闭容器中,加入一定量的CO2和H2,在900℃时发生吸热反应并记录前5min各物质的浓度,第6min改变了条件。各物质的浓度变化如下表;
| 时间/min | CO2(mol·L-1) | H2(mol·L-1) | CO(mol·L-1) | H2O(mol·L-1) |
| 0 | 0.2000 | 0.3000 | 0 | 0 |
| 2 | 0.1740 | 0.2740 | 0.0260 | 0.0260 |
| 5 | 0.0727 | 0.1727 | 0.1273 | 0.1273 |
| 6 | 0.0350 | 0.1350 | 0.1650 |
①前2min,用CO表示的该化学反应的速率为 ▲ ;
②第5—6min,平衡移动的可能原因是 ▲ ;
(4)直接排放煤燃烧产生的烟气会引起严重的环境问题。煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
已知:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ·mol-1
2NO2(g)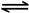 N2O4(g) △H=-56.9 kJ·mol-1
N2O4(g) △H=-56.9 kJ·mol-1
H2O(g) = H2O(l) △H = -44.0 kJ·mol-1
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
▲ 。
(5)在一定条件下,可以用NH3处理NOx。已知NO与NH3发生反应生成N2和H2O,现有NO和NH3的混合物1mol,充分反应后得到的还原产物比氧化产物多1.4 g,则原反应混合物中NO的物质的量可能是 ▲ mol
(6)在一定条件下,也可以用H2处理CO合成甲醇和二甲醚(CH3OCH3)及许多烃类物质。当两者以物质的量11催化反应,其原子利用率达100%,合成的物质可能是 ▲ 。
a.汽油 b.甲醇 c.甲醛 d.乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,跟100mL 0.5mol/L CaCl2溶液所含的Cl-物质的量浓度相同的是
A.100mL 1mol/L MgCl2溶液 B.200mL 0.25mol/L AlCl3溶液
C.200ml 1mol/L NaCl溶液 D.200ml 0.5mol/L HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
质量分数为n的硫酸溶液,其物质的量浓度a mol/L为,加热蒸发水使其质量分数变为2n,此时,该溶液中的物质的量浓度为b mol/L,则与的关系正确的是
A.b=2a B.a=2b C.b﹥2a D.b﹤2a
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中物质的分类组合完全正确的是 ( )
| 编 号 | A | B | C | D |
| 强电解质 | KNO3 | H2SO4 | Ba(OH)2 | BaSO4 |
| 弱电解质 | CH3COOH | CaCO3 | H2S | NH3·H2O |
| 非电解质 | SO2 | CO2 | Cl2 | C2H5OH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是反应CO(g)+2H2(g) = CH3OH(g)进行过程中的能量变化曲线。下列相关说法正确的是 ( )
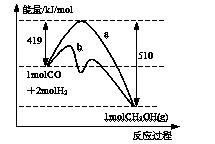
A.该反应是吸热反应 B.使用催化剂后反应热减小
C.热化学方程式为CO(g)+2H2(g) = CH3OH(g) △H=—510 kJ·mol-1
D.曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
超氧化钾和二氧化碳反应生成氧气(4KO2+2CO2===2K2CO3+3O2),在医院、矿井、潜水、高空飞行中用作供氧剂。13.2 L(标准状况)CO2和KO2反应后,气体体积变为18.8 L(标准状况),计算反应消耗的KO2的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中正确的是
A.K37ClO3与浓HCl在加热条件下生成Cl2的化学方程式:
K37ClO3+6HCl=K37Cl+3Cl2↑+3H2O
B.表示H2燃烧热的热化学方程式: H2(g)+ O2(g)=H2O(g) △H= -241.8KJ/mol
O2(g)=H2O(g) △H= -241.8KJ/mol
C.将1~2ml FeCl3饱和溶液滴入到20ml沸水中所发生的离子方程式:
Fe3++3H2O Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
D.电解氯化钠溶液: 2Cl—+2H+ Cl2↑+H2↑
Cl2↑+H2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com