
【题目】向1.00L浓度均为0.0100mol/L的Na2SO3、NaOH 混合溶液中通入HCl气体调节溶液pH(忽略溶液体积变化)。其中比H2SO3、HSO3-、SO32-平衡时的分布系数(各含硫物种的浓度与含硫物种总浓度的比)随HCl气体体积(标况下)的变化关系如图所示(忽略SO2气体的逸出);已知Ka1代表H2SO3在该实验条件下的一级电离常数。下列说法正确的是
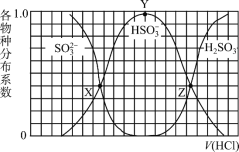
A.Z点处的pH=-lgKa1(H2SO3)
B.从X点到Y点发生的主要反应为SO32- +H2OHSO3- +OH-
C.当V(HCl)≥672mL时,c(HSO3-) = c(SO32-)=0mol/L
D.若将HCl改为NO2,Y点对应位置不变
【答案】A
【解析】
A.在Z点c(H2SO3)=c(HSO3-),由![]() ,则有
,则有![]() ,则pH=-lgc(H+)=-lgKa1,A正确;
,则pH=-lgc(H+)=-lgKa1,A正确;
B.根据图示,从X点到Y点,SO32-的浓度减少,而HSO3-的浓度在增加,则加入盐酸发生的主要反应为SO3-+H+=HSO3,B错误;
C.当V(HCl)=672mL时,n(HCl)=0.672L÷22.4L·mol-1=0.03mol。溶液中的NaOH和Na2SO3的物质的量均为1L×0.01mol·L-1=0.01mol,通入0.03molHCl,NaOH完全反应,Na2SO3转化为H2SO3。H2SO3为弱酸,可经第一二步电离产生HSO3-和SO32-,其关系是c(HSO3-)>c(SO32-)>0,C错误;
D.若将HCl换为NO2,NO2会与水反应,3NO2+H2O=2HNO3+NO,生成的HNO3有强氧化性,可以氧化Na2SO3,溶液中将没有SO32-、HSO3-、H2SO3等粒子,Y点位置会消失,D错误。
答案选A。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】如图是甲醇燃料电池的结构示意图。电池总反应为:2CH3OH+3O2=2CO2+4H2O。下列说法正确的是( )

A.左电极为电池的负极,a处通入的物质是空气
B.右电极为电池的负极,b处通入的物质是甲醇
C.正极反应式为:O2+2H2O-4e-=4OH-
D.负极反应式为:CH3OH+H2O-6e-=CO2+6H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 键和
键和![]() 键的理解不正确的是
键的理解不正确的是![]()
A. ![]() 键可以绕键轴旋转,
键可以绕键轴旋转,![]() 键不能绕键轴旋转
键不能绕键轴旋转
B. ![]() 分子中的
分子中的![]() 键是
键是![]()
![]() 键,HClO分子中的
键,HClO分子中的![]() 键都是
键都是![]()
![]() 键
键
C. ![]() 分子和
分子和![]() 中都是含有5个
中都是含有5个![]() 键
键
D. ![]() 键以“头碰头”方式重叠,
键以“头碰头”方式重叠,![]() 键以“肩并肩”方式重叠
键以“肩并肩”方式重叠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金晶体采取面心立方最密堆积。设金原子的直径为d,用NA表示阿伏加德罗常数,M表示金的摩尔质量。则下列说法错误的是( )
A.金晶体每个晶胞中含有4个金原子
B.金属键无方向性,金属原子尽可能采取紧密堆积
C.一个晶胞的体积是![]()
D.金晶体的密度是![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X的某价态离子Xn+中所有电子正好充满K、L、M三个电子层,它与N3-形成的晶体的晶胞结构如图所示。
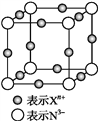
(1)该晶体的阳离子与阴离子个数比为____。
(2)该晶体中Xn+中n=____。
(3)X元素的原子序数是_____。
(4)晶体中每个N3-被____个等距离的Xn+包围。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇在保健品领域有广泛的应用。其合成路线如下:
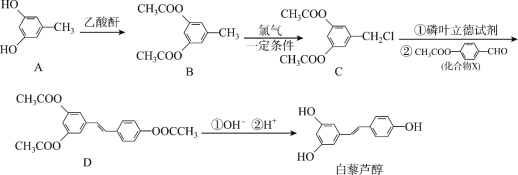
回答下列问题:
(1)物质B中含氧官能团的名_______。B→C的反应类型为___________。
(2)1mol有机物D最多能消耗NaOH为 _________mol,白藜芦醇遇足量浓溴水时反应的化学方程式为____________。
(3)已知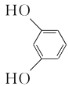 的系统名称1,3-苯二酚,则A的名称为________,已知乙酸酐(
的系统名称1,3-苯二酚,则A的名称为________,已知乙酸酐(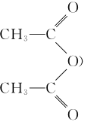 )极易与水反应生成乙酸,是很好的吸水剂。试从平衡移动的角度分析A→B反应中用乙酸酐代替乙酸的目的是__________。
)极易与水反应生成乙酸,是很好的吸水剂。试从平衡移动的角度分析A→B反应中用乙酸酐代替乙酸的目的是__________。
(4)C的核磁共振氢谱有_________组峰,写出满足下列条件的化合物X的所有同分异构体的结构简式__________。
①具有与X相同的官能团②属于醋酸酯
(5)利用甲苯、磷叶立德试剂和乙醛为原料可以合成![]() (涉及无机试剂自选),请写出合成路线__________。
(涉及无机试剂自选),请写出合成路线__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素ⅹ位于第4周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2;元素Y基态原子的3p轨道上有4个电子。X与Y形成的化合物的晶胞结构如图所示,下列关于该晶体的说法正确的是( )
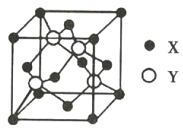
A.1个晶胞中所含离子总数为18
B.X2+的配位数为8,Y2-的配位数为4
C.与每个X2+距离最近且相等的X2+共有12个
D.该化合物的化学式为CaS
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】配制250mL一定物质的量浓度的盐酸,并用该盐酸滴定未知浓度的NaOH溶液,下列实验操作或说法错误的是
A.实验前,容量瓶和酸式滴定管都需要检查是否漏液
B.若NaOH溶液因久置而变质(含少量Na2CO3),用甲基橙作指示剂,对滴定结果无影响
C.若配制盐酸标准溶液定容时俯视刻度线,则所测定NaOH溶液的浓度偏小
D.当最后一滴盐酸标准液滴入锥形瓶中,溶液颜色由黄色变为橙色时,即达滴定终点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列推论错误的是
A.NaCl为离子晶体,可推测CsCl也为离子晶体
B.CO2晶体是分子晶体,可推测CS2晶体也是分子晶体
C.NH4+为正四面体结构,可推测PH4+也为正四面体结构
D.NCl3中N原子是sp3杂化,可推测BCl3中B原子也是sp3杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com