
| A. | ③④ | B. | ①②③④ | C. | ①③④ | D. | 全部 |
科目:高中化学 来源: 题型:解答题
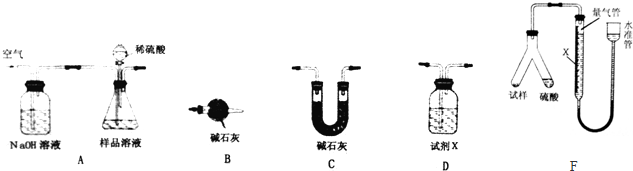
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 上述实验证明氧化性:MnO4->Cl2>Fe3+ | |
| B. | 上述实验中,有一个氧化还原反应 | |
| C. | 实验①生成的气体需要进行尾气处理 | |
| D. | 实验②证明Fe2+既有氧化性又有还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 保存氢氧化钠溶液,常用带橡胶塞的玻璃瓶 | |
| B. | 保存浓硝酸,常用带玻璃塞的棕色试剂瓶 | |
| C. | 保存金属铝时,常在试剂瓶中加入煤油进行封存 | |
| D. | 保存氢氟酸时,常用塑料瓶而不用玻璃瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠的化学式:Na2O | |
| B. | 氯化钙化学式:CaCl | |
| C. | 铝的原子结构示意图: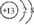 | |
| D. | 硫酸钠的电离方程式:Na2SO4═2Na++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 离子 | Mg2+ | Al3+ | Cl- | X |
| 物质的量浓度 | a | 2a | 2a | b |
| A. | Na+、6a | B. | SO42-、3a | C. | OH-、6a | D. | CO32-、4a |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,100g 17%H2O2水溶液中含氧原子总数为NA | |
| B. | 常温常压下,2.8g N2气体分子中所含的共用电子对数目为0.3NA | |
| C. | 0.2mol/L的NaCl溶液中含有的Cl-数是0.2NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com