
| A、可逆反应的特征是正反应速率和逆反应速率相等 |
| B、对已达到化学平衡的反应仅改变浓度,若平衡移动,则平衡常数(K)一定不变 |
| C、电镀时应把镀件置放电解槽的阳极 |
| D、电解AlCl3来制取金属铝 |


科目:高中化学 来源: 题型:
| A、NaOH |
| B、HCl |
| C、CaCO3(固体) |
| D、H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、500 mL,1 mol/L MgCl2溶液中含有Cl-数目为0.5NA |
| B、标准状况下,1mol CCl4与1mol O2所占的体积相等 |
| C、17g NH3含有的电子个数为l0NA |
| D、36g H2O与32g CH4所含的氢原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、Cl-、K+、SiO32- |
| B、Na+、CO32-、Fe2+、NO3- |
| C、K+、SO42-、Cl-、Cu2+ |
| D、Na+、NO3-、Al3+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、100℃时,将pH=2的盐酸与pH=12的NaOH溶液等体积混合,溶液显中性 |
| B、25℃时,某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 |
| C、25℃时,pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍 |
| D、100℃时某溶液中由水电离产生的c(H+)=1×10-11mol?L-1,则该溶液的pH可能是11或3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、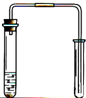 用铜和稀硝酸制取少量NO |
B、 制取并收集氨气 |
C、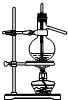 蒸馏法分离水和酒精 |
D、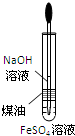 制备Fe(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
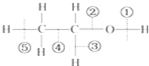 乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说明是:
乙醇分子中的各种化学键如图所示,关于乙醇在各种反应中断裂键的说明是:查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com