
��8�֣�80��ʱ����0.40mol��N2O4�������2L�Ѿ���յĹ̶��ݻ����ܱ������У��������·�Ӧ��N2O4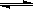 2NO2 ��H>0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
2NO2 ��H>0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
| ʱ�䣨s�� n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
��0.0020mol/(L.s) ��1.8 �۱�dz ��D
��������������ٷ�Ӧ���е�20sʱ������NO2��0.24mol��������N2O4��0.12mol������a��0.28mol�����20s��40s����N2O4�仯����0.08mol�������䷴Ӧ������0.08mol��2L��20s��0.002 mol/(L��s)��
�ڸ��ݱ������ݿ�֪��ƽ��ʱNO2�����ʵ�����0.60mol������N2O4�����ʵ�����0.40mol��0.30mol��0.10mol����Ũ�ȷֱ���0.30mol/L��0.05mol/L�������ƽ�ⳣ����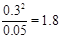 ��
��
�����ڷ�Ӧ�����ȷ�Ӧ�����Խ����¶ȣ�ƽ�����淴Ӧ�����ƶ���NO2��Ũ�ȼ�С����ɫ��dz��
��ƽ�ⳣ��ֻ���¶��й�ϵ�����������¶ȣ�ƽ��������Ӧ�����ƶ�������ƽ�ⳣ������
���㣺��ѧƽ��
�����������ۺ��Խ�ǿ�����dz���������Ҫ�ӻ���֪ʶ���ǡ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��6�֣���80��ʱ����0.40 mol N2O4�������2 L�Ѿ���յĹ̶��ݻ����ܱ������з�����ӦN2O4��g��2NO2��g�� ��H= +57 kJ��mol��1����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4)/mol | 0.40 | a | 0.20 | c | d | e |
| n(NO2)/mol | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
��1������a = �����¶�ʱ�÷�Ӧ��ƽ�ⳣ��K= ��
��2���ı�����ʹ��Ӧ���´ﵽƽ�⣬��ʹc(NO2)/c(N2O4)ֵ��С�Ĵ�ʩ�У�����ţ� ��
A������N2O4����ʼŨ�� B�������¶�
C��ʹ�ø�Ч���� D������������ͨ��ϡ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��12�֣���80��ʱ����0.40 mol��N2O4�������1 L�̶��ݻ����ܱ������з�����Ӧ��N2O4 2 NO2����H ��0����ÿ��һ��ʱ��������ڵ����ʽ��вⶨ���õ��������ݣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 | 100 |
| n��N2O4����mol�� | 0.40 | a | 0.20 | c | d | e |
| n��NO2����mol�� | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
��1����20s �� 40s֮�䣬��N2O4��ʾ��ƽ����Ӧ����Ϊ ��
��2����80��ʱ�÷�Ӧ��ƽ�ⳣ��K�� ��
��3��Ҫ����÷�Ӧ��ƽ�ⳣ�����ɲ�ȡ�Ĵ�ʩ�У�����ţ� ��
������N2O4����ʼŨ�� ������������ͨ��NO2
��ʹ�ø�Ч���� �������¶�
��4����Ӧ������100s���������¶ȣ�����������ɫ �����dz������������䡱����
��5����Ӧ������100s�������������ٳ���0.40 mol��N2O4���壬��ﵽ��ƽ���N2O4��ת���ʽ� �����������С�����䡱����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�������ʡ����������ѧ������ĩ���Ի�ѧ�Ծ� ���ͣ������
��6�֣���80��ʱ����0.40 mol N2O4�������2 L�Ѿ���յĹ̶��ݻ����ܱ������з�����ӦN2O4��g�� 2NO2��g����H=" +57" kJ��mol��1����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
2NO2��g����H=" +57" kJ��mol��1����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
| ʱ�䣨s�� | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4)/mol | 0.40 | a | 0.20 | c | d | e |
| n(NO2)/mol | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��㶫ʡ÷���и߶���ѧ���п����������⣨��ѧ���֣� ���ͣ������
(20��)��80 ��ʱ����0.40 mol��N2O4�������2 L�Ѿ���յĹ̶��ݻ����ܱ������У��������·�Ӧ��N2O4��g�� 2NO2��g����H >0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
2NO2��g����H >0����һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
|
ʱ��/s
n/mol |
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)����20~40 s����N2O4��ʾ��ƽ����Ӧ����Ϊ____________mol�� L��1��s��1��
(2)������80 ��ʱ�÷�Ӧ��ƽ�ⳣ��K=___________��
(3)��Ӧ������100 s��Ӧ�������¶Ƚ��ͣ�����������ɫ___________(���dz����������䡱)��
(4)Ҫ����÷�Ӧ��Kֵ���ɲ�ȡ�Ĵ�ʩ��___________(�����)��
A.����N2O4����ʼŨ�� B.����������ͨ��NO
C.ʹ�ø�Ч���� D.�����¶�
(5)��ͼ��80 ��ʱ������N2O4���ʵ����ı仯���ߣ����ڸ�ͼ�в������÷�Ӧ��60 ��ʱN2O4���ʵ����ı仯���ߡ�
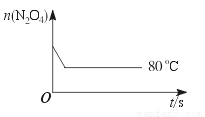
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012�찲��ʡ�����и߶���ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ������
��12�֣���80��ʱ����0.40 mol��N2O4�������1 L�̶��ݻ����ܱ������з�����Ӧ��N2O4  2 NO2����H ��0����ÿ��һ��ʱ��������ڵ����ʽ��вⶨ���õ��������ݣ�
2 NO2����H ��0����ÿ��һ��ʱ��������ڵ����ʽ��вⶨ���õ��������ݣ�
|
ʱ�䣨s�� |
0 |
20 |
40 |
60 |
80 |
100 |
|
n��N2O4����mol�� |
0.40 |
a |
0.20 |
c |
d |
e |
|
n��NO2����mol�� |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
��1����20s �� 40s֮�䣬��N2O4��ʾ��ƽ����Ӧ����Ϊ ��
��2����80��ʱ�÷�Ӧ��ƽ�ⳣ��K�� ��
��3��Ҫ����÷�Ӧ��ƽ�ⳣ�����ɲ�ȡ�Ĵ�ʩ�У�����ţ� ��
������N2O4����ʼŨ�� ������������ͨ��NO2
��ʹ�ø�Ч���� �������¶�
��4����Ӧ������100s���������¶ȣ�����������ɫ �����dz������������䡱����
��5����Ӧ������100s�������������ٳ���0.40 mol��N2O4���壬��ﵽ��ƽ���N2O4��ת���ʽ� �����������С�����䡱����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com