
| A、①③⑤ | B、②⑤ |
| C、②③⑤ | D、①③④ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、钠在空气中燃烧产生黄色火焰,生成淡黄色固体物质 |
| B、新制氯水呈浅黄绿色,氯水放置数天后pH将变大 |
| C、铁与稀盐酸反应生成氯化亚铁,而铁与氯气反应则生成三氯化铁 |
| D、漂白粉的有效成分是次氯酸钙,它具有漂白性是因为在水溶液中生成了有强氧化性的次氯酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
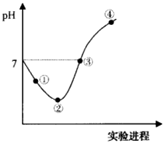 常温下将氯气通入水中至饱和,然后向所得饱和氯水中逐滴滴加0.1 mol?L-1 NaOH溶液,整个过程中pH变化如图所示,下列有关叙述不正确的是( )
常温下将氯气通入水中至饱和,然后向所得饱和氯水中逐滴滴加0.1 mol?L-1 NaOH溶液,整个过程中pH变化如图所示,下列有关叙述不正确的是( )| A、NaOH与Cl2恰好完全反应时水的电离程度最大 |
| B、实验过程中的pH溶液的不能用pH试纸测得 |
| C、②点之前溶液中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) |
| D、②~③之间所发生反应的离子方程式:Cl2+OH-═Cl-+ClO-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
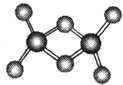 科学家合成了一种稳定的氢铝化合物,其熔点为150℃,可用作高能燃料或储氢材料.Al2H6的球棍模型如图所示.下列说法不正确的是( )
科学家合成了一种稳定的氢铝化合物,其熔点为150℃,可用作高能燃料或储氢材料.Al2H6的球棍模型如图所示.下列说法不正确的是( )| A、Al2H6可以燃烧,产物为氧化铝和水 |
| B、Al2H6是共价化合物 |
| C、Al2H6中所有原子在同一平面 |
| D、Al2H6是非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3能与碱反应,食品工业上用作焙制糕点的膨松剂 |
| B、MgO、Al2O3的熔点很高,可制作耐高温材料 |
| C、Al具有良好的延展性和抗腐蚀性,可制成铝箔包装物品 |
| D、铜盐能使蛋白质变性,游泳场馆常用硫酸铜作池水消毒剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、HClO的电子式为: |
B、CH4分子的球棍模型: |
| C、甲酸甲酯的实验式:CH2O |
| D、2-戊烯的结构简式:CH3CH2CH=CHCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
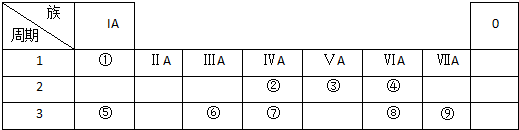
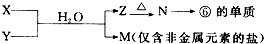
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com