
 ?
?
图13-4
(1)在大试管中配置一定比例的乙醇、乙酸和浓硫酸的混合液的方法是 ,然后轻轻振荡试管,使之混合均匀。?
(2)加入浓硫酸的目的是 。?
(3)饱和碳酸钠溶液的作用是 。?
(4)实验生成的乙酸乙酯,其密度比水 (填“大”或“小”),有 气味。?
(5)若实验中反应温度不当,使反应温度维持在140 ℃左右,此时主要有机副产物是 。?
(6)与教材采用的实验装置不同,这位老师采用球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中,在此处,球形干燥管的作用有① ;?② 。?
科目:高中化学 来源: 题型:

| H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
名称 | 密度/g·cm-3 | 沸点/℃ | 溶解性 |
苯甲酸 | 1.265 9 | 249 | 微溶于水、易溶于有机溶剂 |
甲醇 | 0.791 5 | 64.65 | 易溶于水、易溶于有机溶剂 |
苯甲酸甲酯 | 1.093 7 | 199 | 难溶于水、易溶于有机溶剂 |
硫酸 | 1.834 | 338 | 易溶于水 |
(1)某同学用如下图一所示的装置制备苯甲酸甲酯,结果发现锥形瓶中没有收集到苯甲酸甲酯,原因是____________________________________________________________________。

(2)该同学在分析实验失败的原因后,决定改用图二的装置进行,向烧瓶中加入浓硫酸、15 g苯甲酸、20 mL甲醇和_________________,冷却水从_________________处进。
(3)反应一段时间后,取下烧瓶,冷却后向其中加入一定量的水,分液,将分液漏斗_________________ (填“上”或“下”)层中的液体移入装有少量固体碳酸钠的锥形瓶中,过滤,碳酸钠的作用是_________________。
(4)将滤液倒入蒸馏装置中进行蒸馏,温度计应如何放置______________________________。
(5)将得到的苯甲酸甲酯进行称量,质量为13.6 g,则苯甲酸的转化率为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
某校兴趣小组对氢氧化钠溶液和稀盐酸混合后的有关问题,进行了如下探究:
Ⅰ.(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如图所示
实验。
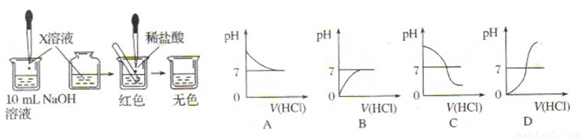
X溶液是 ,滴入的量一般为 。
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应。在盛有氢氧化钠溶液的试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
①写出测定溶液pH的方法: 。
②上图中哪个图像符合该同学的记录 (填序号)。
(3)你认为甲、乙两位同学的实验中, (填“甲同学”、“乙同学”或“甲、乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由: 。
Ⅱ.丙同学测出10mL 10%的NaOH溶液和不同体积的10%的盐酸溶液混合过程中,溶液的温度变化见下表(假设两溶液密度相同)。
| 加入盐酸的 体积( | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 溶液温度上升 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 |
就此实验回答:
(4)盐酸和氢氧化钠的反应是 (填“吸热”或“放热”)反应。
(5)请在图中绘制出溶液的温度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。
Ⅲ.丁同学为测定标示质量分数为32%的盐酸的实际质量分数,用pH测定仪组成实验装置。实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加入该盐酸,pH测定仪打印出加入盐酸的质量与烧杯中溶液的pH关系如图所示。
(6)请以此次测定的结果为依据计算该盐酸的实际质量分数为 。
(7)请分析你的计算结果与标签标示的质量分数不一致的可能原因(若一致,此空可不填): 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省高三5月模拟(理综)化学部分 题型:填空题
某校兴趣小组对氢氧化钠溶液和稀盐酸混合后的有关问题,进行了如下探究:
Ⅰ.(1)甲同学为了证明氢氧化钠溶液与稀盐酸能够发生反应,设计并完成了如图所示
实验。
X溶液是 ,滴入的量一般为 。
(2)乙同学也设计完成了另一个实验,证明氢氧化钠溶液与盐酸能够发生反应。在盛有氢氧化钠溶液的试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
①写出测定溶液pH的方法: 。
②上图中哪个图像符合该同学的记录 (填序号)。
(3)你认为甲、乙两位同学的实验中, (填“甲同学”、“乙同学”或“甲、乙两同学”)的实验能充分证明氢氧化钠溶液与盐酸发生了反应,请说明理由: 。
Ⅱ.丙同学测出10mL 10%的NaOH溶液和不同体积的10%的盐酸溶液混合过程中,溶液的温度变化见下表(假设两溶液密度相同)。
|
加入盐酸的 体积( |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
18 |
|
溶液温度上升 |
5.2 |
9.6 |
12.0 |
16.0 |
18.2 |
16.7 |
15.7 |
14.7 |
13.7 |
就此实验回答:
(4)盐酸和氢氧化钠的反应是 (填“吸热”或“放热”)反应。
(5)请在图中绘制出溶液的温度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。
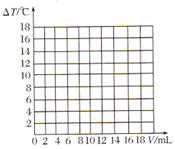
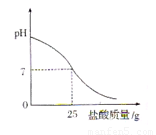
Ⅲ.丁同学为测定标示质量分数为32%的盐酸的实际质量分数,用pH测定仪组成实验装置。实验时先在烧杯中加入20g 40%的氢氧化钠溶液,再逐滴加入该盐酸,pH测定仪打印出加入盐酸的质量与烧杯中溶液的pH关系如图所示。
(6)请以此次测定的结果为依据计算该盐酸的实际质量分数为 。
(7)请分析你的计算结果与标签标示的质量分数不一致的可能原因(若一致,此空可不填): 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com