
 ŅŃÖŖpAg=-lg£ØAg+£©£¬Ksp£ØAgCl£©=1”Į10-12£®ČēĶ¼ŹĒĻņ10ml AgNO3ČÜŅŗÖŠÖš½„¼ÓČė0.1mol/LµÄNaClČÜŅŗŹ±£¬ČÜŅŗµÄpAgĖę׿ÓČėNaClČÜŅŗµÄĢå»ż±ä»ÆµÄĶ¼Ļó£ØŹµĻߣ©£®øł¾ŻĶ¼ĻóĖłµĆĻĀĮŠ½įĀŪÕżČ·µÄŹĒ[ĢįŹ¾£ŗKsp£ØAgCl£©£¾Ksp£ØAgI£©]£Ø””””£©
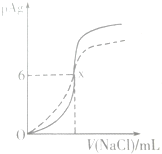
ŅŃÖŖpAg=-lg£ØAg+£©£¬Ksp£ØAgCl£©=1”Į10-12£®ČēĶ¼ŹĒĻņ10ml AgNO3ČÜŅŗÖŠÖš½„¼ÓČė0.1mol/LµÄNaClČÜŅŗŹ±£¬ČÜŅŗµÄpAgĖę׿ÓČėNaClČÜŅŗµÄĢå»ż±ä»ÆµÄĶ¼Ļó£ØŹµĻߣ©£®øł¾ŻĶ¼ĻóĖłµĆĻĀĮŠ½įĀŪÕżČ·µÄŹĒ[ĢįŹ¾£ŗKsp£ØAgCl£©£¾Ksp£ØAgI£©]£Ø””””£©| A£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬AgClŌŚ“æĖ®ŗĶŌŚNaClČÜŅŗÖŠµÄČܽā¶ČĻąµČ | |
| B£® | ŌAgNO3ČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ0.1mol/L | |
| C£® | Ķ¼ÖŠxµÄ×ų±źĪŖ£Ø100£¬6£© | |
| D£® | 0.1mol/LµÄNaClČÜŅŗ»»³É0.1mol/LµÄNaIČÜŅŗŹ±£¬Ķ¼Ļó±äĪŖŠéĻß²æ·Ö |
·ÖĪö A£®ĀČĄė×ÓÅØ¶Č“óŠ”Ó°ĻģĀČ»ÆŅųµÄČܽā¶Č£»
B£®øł¾ŻpAg=-lg{c£ØAg+£©}Ēó³öAg+µÄÅØ¶Č£»
C£®xµćc£ØAg+£©=10-6 mol•L-1£¬øł¾ŻĻõĖįŅųµÄĮæĒó³öĻūŗĵÄĀČ»ÆÄĘ£»
D£®ÓÉÓŚKsp£ØAgI£©øüŠ”£¬ĖłŅŌc£ØAg+£©øüŠ”£®
½ā“š ½ā£ŗA£®ČÜŅŗÖŠĀČĄė×ÓÅضČŌ½“ó£¬ĀČ»ÆŅųµÄČܽā¶ČŌ½Š”£¬ŌņAgClŌŚĖ®ÖŠµÄČܽā¶Č½Ļ“󣬹ŹA“ķĪó£»
B£®Ķ¼ÖŠŌµćpAg=0£¬ŌņAg+µÄÅضČĪŖ£ŗc£ØAg+£©=100 mol•L-1£¬¼“ŌAgNO3ČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖ1 mol•L-1£¬¹ŹB“ķĪó£»
C£®xµćc£ØAg+£©=10-6 mol•L-1£¬Ņ»°ćČĻĪŖČÜŅŗÖŠĄė×ÓÅØ¶ČŠ”ÓŚ10-5 mol•L-1£¬¼“³ĮµķĶźČ«£¬ŌņAgNO3ÓėNaClĒ”ŗĆ·“Ó¦£¬n£ØNaCl£©=n£ØAgNO3£©=0.01L”Į1mol•L-1=0.01mol£¬ĖłŅŌV£ØNaCl£©=100mL£¬¼“xµćµÄ×ų±źĪŖ£Ø100£¬6£©£¬¹ŹCÕżČ·£»
D£®ÓėAgClĻą±Č£¬µā»ÆŅųµÄKsp£ØAgI£©øüŠ”£¬ĖłŅŌ°Ń0.1 mol•L-1µÄNaCl»»³É0.1mol•L-1NaI£¬ŌņČÜŅŗÖŠc£ØAg+£©øüŠ”£¬ŌņpAgøü“ó£¬Ķ¼Ļó²»·ū£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖAgClµÄKspµÄÓ¦ÓĆ£¬ĪŖøßĘµæ¼µć£¬×¢Ņā°ŃĪÕĢāøÉÖŠµÄŠÅĻ¢£¬æ¼²éѧɜ·ÖĪöĢāÄæŠÅĻ¢²¢ÓĆÓŚ½ā¾öĪŹĢāµÄÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2a=3b | |
| B£® | 7b=4a | |
| C£® | Ō»ģŗĻĘųĢåÖŠV£ØH2£©=bL£¬V£ØO2£©=£Øa-b£©L | |
| D£® | Ō»ģŗĻĘųĢåÖŠV£ØH2£©=2£Øa-b£©L£¬V£ØO2£©=£Ø2b-a£©L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗ¬µāĮæ½Ļøß | B£® | ŗ¬ĮņĮæ½Ļøß | C£® | ŗ¬¹ÆĮæ½Ļøß | D£® | ŗ¬·śĮæ½Ļøß |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

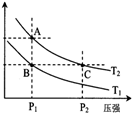
| A£® | Ē°5min·“Ó¦µÄĘ½¾łĖŁĀŹv£ØNO£©=0.24mol•£ØL•min£©-1 | |
| B£® | T”ꏱ·“Ó¦¢ŁµÄ»ÆŃ§Ę½ŗā³£ŹżK=0.36 | |
| C£® | 10minŹ±øı䷓ӦĢõ¼žæÉÄÜŹĒ½µµĶĪĀ¶Č | |
| D£® | ČōĘšŹ¼Ź±ĻņøĆČŻĘ÷ÖŠ³äČė1.6mol NO2ŗĶ4.0mol N2O4£¬T”ę“ļµ½Ę½ŗāŹ±£¬NO2µÄĪļÖŹµÄĮæÅضČÓėĶ¼ÖŠ5”«10minµÄ²»Ķ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¼×“¼ŹĒŅ»ÖÖæÉŌŁÉśÄÜŌ“£¬¾ßÓŠæŖ·¢ŗĶÓ¦ÓĆµÄ¹ćĄ«Ē°¾°£¬¹¤ŅµÉĻŅ»°ćæɲÉÓĆČēĻĀ·“Ó¦Ą“ŗĻ³É¼×“¼£ØÓŚ¹Ģ¶ØČŻĘ÷ÖŠ½ųŠŠ£©£ŗ2H2£Øg£©+CO£Øg£©?CH3OH£Øg£©
¼×“¼ŹĒŅ»ÖÖæÉŌŁÉśÄÜŌ“£¬¾ßÓŠæŖ·¢ŗĶÓ¦ÓĆµÄ¹ćĄ«Ē°¾°£¬¹¤ŅµÉĻŅ»°ćæɲÉÓĆČēĻĀ·“Ó¦Ą“ŗĻ³É¼×“¼£ØÓŚ¹Ģ¶ØČŻĘ÷ÖŠ½ųŠŠ£©£ŗ2H2£Øg£©+CO£Øg£©?CH3OH£Øg£©| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Į½ĒåŅŗ»ģŗĻ£¬AgClŗĶAgI¶¼³Įµķ | |
| B£® | ĻņAgIĒåŅŗ¼ÓČėAgNO3£¬c£ØAg+£©Ōö“ó£¬KSp£ØAgI£©Ņ²Ōö“ó | |
| C£® | ČōČ”0.1435æĖAgCl¹ĢĢå·ÅČė100mLĖ®£ØŗöĀŌĢå»ż±ä»Æ£©£¬c£ØCl-£©ĪŖ0.01mol/L | |
| D£® | ČōAgNO3×ćĮ棬AgClŗĶAgI¶¼æɳĮµķ£¬µ«ŅŌAgClĪŖÖ÷ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆAgI½ŗĮ£“ųÕżµēŗÉ | |
| B£® | øĆAgI½ŗĢå“ųøŗµēŗÉ | |
| C£® | øĆAgI½ŗĢå½ųŠŠµēÓ¾Ź±£¬½ŗĮ£ĻņŃō¼«ŅĘ¶Æ | |
| D£® | øĆAgI½ŗĢåŹĒµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+”¢K+”¢CO32-”¢NO3- | B£® | K+”¢MnO4-”¢NH4+”¢NO3- | ||
| C£® | NH4+”¢SO42-”¢Al3+”¢NO3- | D£® | Na+”¢Ca2+”¢NO3-”¢CO32- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com