
 .
. 分析 (1)由密度可确定有机物的相对分子质量,进而计算9.0g有机物的物质的量,计算生成二氧化碳、水的物质的量,确定1mol有机物含有C、H、O的个数,可确定有机物分子式;
(2)根据N的不饱和度及核磁共振氢谱显示的峰面积之比确定N的结构简式,然后写出与钠反应的化学方程式;
(3)M是高分子化合物,通过水解得到N,据此确定M的结构简式.
解答 解:(1)N的摩尔质量为:M(N)=4.02g/L×22.4L/mol=90g/mol,n(N)=$\frac{9g}{90g/mol}$=0.1mol/L,
1molN中:n(C)=$\frac{\frac{13.2g}{44g/mol}}{0.1mol}$=3、n(H)=$\frac{\frac{5.4g}{18g/mol}×2}{0.1mol}$=6、n(O)=$\frac{90-12×3-1×6}{16}$=3,
则有机物的分子式为:C3H6O3,
故答案为:C3H6O3;
(2)C3H6O3的不饱和度为:$\frac{3×2+2-6}{2}$=1,N分子中含有1个不饱和键,N的核磁共振氢谱显示的峰面积之比为1:1:1:3,该有机物分子中含有4种H,其中3应该为甲基,由于N分子中含有3个O、3个C,则其分子中应该含有1个羟基、1个羧基,其结构简式为:CH3CH(OH)COOH,N与钠反应的化学方程式为:CH3CH(OH)COOH+2Na→CH3CH(ONa)COONa+H2↑,
故答案为:CH3CH(OH)COOH+2Na→CH3CH(ONa)COONa+H2↑;
(3)M最终水解得到CH3CH(OH)COOH,则M是CH3CH(OH)COOH通过缩聚反应生成的高分子化合物,则M的结构简式为: ,
,
故答案为: .
.
点评 本题考查了有机物的计算与推断,为高考常见题型,题目难度中等,明确常见有机物结构与性质为解答关键,试题侧重于学生的分析、计算能力的考查.


科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与稀硝酸反应:2Fe3O4+18H+═6Fe3++H2↑+ 8H2O | 正确 |
| B | 向碳酸镁中加稀盐酸:CO${\;}_{3}^{2-}$+2H+═CO2↑+ H2O | 错误,碳酸镁不应写成离子形式 |
| C | 向硫酸铵溶液中加入氢氧化钡溶液:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++4Cl-+ Br2 | 错误,Fe2+与Br-的化学计量数之比应为1:2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
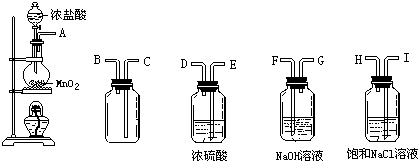
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴元素只存在于海洋中,故溴被称为“海洋元素” | |
| B. | 硅单质是一种半导体材料,也常用于制造光导纤维 | |
| C. | 钠在盛有氯气的集气瓶中燃烧,火焰呈苍白色,瓶口有白烟 | |
| D. | 工业炼铁过程加入石灰石的作用是除脉石(SiO2)造渣 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 编号 | 信 息 | 晶体类型 |
| A | 沸点低,易溶于水,水溶液能导电 | 离子晶体 |
| B | 熔点630.74℃,沸点1750℃,液态能导电 | 分子晶体 |
| C | 熔点3410℃,硬度大,固体不能导电 | 金属晶体 |
| D | 由共价键结合成空间网状结构的晶体,熔点高、硬度大,固体不能导电 | 原子晶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为工业上氯碱工业的电解槽示意图,据图回答:
如图为工业上氯碱工业的电解槽示意图,据图回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com