
øł¾ŻŅŌĻĀ3øöČČ»Æѧ·½³ĢŹ½£ŗ
2H2S£Øg£©+3O2£Øg£©=2SO2£Øg£©+2H2O£Øl£©”÷H=﹣Q1 kJ/mol
2H2S£Øg£©+O2£Øg£©=2S£Øs£©+2H2O£Øl£©”÷H=﹣Q2 kJ/mol
2H2S£Øg£©+O2£Øg£©=2S£Øs£©+2H2O£Øg£©”÷H=﹣Q3 kJ/mol
ÅŠ¶ĻQ1”¢Q2”¢Q3ČżÕß¹ŲĻµÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | Q1£¾Q2£¾Q3 | B£® | Q1£¾Q3£¾Q2 | C£® | Q3£¾Q2£¾Q1 | D£® | Q2£¾Q1£¾Q3 |
æ¼µć£ŗ
·“Ó¦ČČµÄ“óŠ”±Č½Ļ£®
×ØĢā£ŗ
»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ£®
·ÖĪö£ŗ
Čżøö·“Ó¦¶¼ĪŖ·ÅČČ·“Ó¦£¬ĪļÖŹ·¢Éś»Æѧ·“Ó¦Ź±£¬Éś³ÉŅŗĢ¬Ė®±ČÉś³ÉĘųĢ¬Ė®·Å³öµÄČČĮæ¶ą£¬·“Ó¦Ō½ĶźČ«£¬·Å³öµÄČČĮæŌ½¶ą£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š£ŗ
½ā£ŗŅŃÖŖ¢Ł2H2S£Øg£©+3O2£Øg£©=2SO2£Øg£©+2H2O£Øl£©”÷H=﹣Q1 kJ/mol£¬
¢Ś2H2S£Øg£©+O2£Øg£©=2S £Øs£©+2H2O£Øl£©”÷H=﹣Q2 kJ/mol£¬
¢Ū2H2S£Øg£©+O2£Øg£©=2S £Øs£©+2H2O£Øg£©”÷H=﹣Q3kJ/mol£¬
¢ŁÓė¢ŚĻą±Č½Ļ£¬ÓÉÓŚS”śSO2·ÅČČ£¬ŌņQ1£¾Q2£¬
¢ŚÓė¢ŪĻą±Č½Ļ£¬ÓÉÓŚH2O£Øl£©”śH2O£Øg£©ĪüČČ£¬ŌņQ2£¾Q3£¬
ŌņQ1£¾Q2£¾Q3£¬
¹ŹŃ”A£®
µćĘĄ£ŗ
±¾Ģā漲鷓ӦČČµÄ“óŠ”±Č½Ļ£¬ĢāÄæÄѶČÖŠµČ£¬±¾Ģā×¢Ņā“ÓĪļÖŹ·“Ó¦µÄ³Ģ¶ČŅŌ¼°ĪļÖŹµÄ¾Ū¼ÆדĢ¬µÄ½Ē¶Č±Č½Ļ·“Ó¦ČČµÄ“óŠ”£®


 ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø
ŠĀæĪ±ź½×ĢŻŌĶĮѵĮ·ĻµĮŠ“š°ø æŚĖćŠÄĖćĖŁĖćÓ¦ÓĆĢāĻµĮŠ“š°ø
æŚĖćŠÄĖćĖŁĖćÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠĶØČėX²¢·¢Éś·“Ó¦£ŗ2X(g) Y(g)£¬ĪĀ¶ČT1”¢T2ĻĀXµÄĪļÖŹµÄĮæÅضČc(X)Ėꏱ¼ät±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
Y(g)£¬ĪĀ¶ČT1”¢T2ĻĀXµÄĪļÖŹµÄĮæÅضČc(X)Ėꏱ¼ät±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£¬ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®øĆ·“Ó¦½ųŠŠµ½Mµć·Å³öµÄČČĮæ“óÓŚ½ųŠŠµ½Wµć·Å³öµÄČČĮæ
B£®T2ĻĀ£¬ŌŚ0”«t1Ź±¼äÄŚ£¬v(Y)£½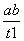 mol·L£1·min£1
mol·L£1·min£1
C£®MµćµÄÕż·“Ó¦ĖŁĀŹvÕż“óÓŚNµćµÄÄę·“Ó¦ĖŁĀŹvÄę
D£®MµćŹ±ŌŁ¼ÓČėŅ»¶ØĮæY£¬Ę½ŗāŗóXĢå»ż·ÖŹżÓėŌĘ½ŗāĻą±ČŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
2008Äź10ŌĀ8ČÕ£¬Čšµä»Ź¼ŅæĘѧŌŗŠū²¼ĆĄ¼®»ŖŅįæĘѧ¼ŅĒ®ÓĄ½”»ńµĆ2008Äź¶Čŵ±“¶ū»Æѧ½±£®ÉŁÄźŹ±“ś£¬Ėū¾Ķ¶Ō»Æѧ²śÉśĮĖÅØŗńµÄŠĖȤ£®16ĖźŹ±£¬ĖūĘ¾½čŅ»øö½šŹōŅ׏ÜĮņĒčĖįŃĪøÆŹ“µÄµ÷²éĻīÄæ£¬ČŁ»ń¾ßÓŠ”°ÉŁÄźÅµ±“¶ū½±”±Ö®³ĘµÄÖųĆū½±Ļī£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
A£®½šŹōøÆŹ“¾ĶŹĒ½šŹōŹ§Č„µē×Ó±»»¹ŌµÄ¹ż³Ģ
B£®½«Ė®æāÖŠµÄĖ®Õ¢£Øøְ壩ÓėĶā¼ÓÖ±½ÓµēŌ“µÄøŗ¼«ĻąĮ¬£¬Õż¼«Į¬½Óµ½Ņ»æé·ĻĢśÉĻæÉ·ĄÖ¹Ė®Õ¢±»øÆŹ“
C£®ÓÉŌµē³ŲŌĄķÖŖĖłÓŠµÄŗĻ½š¶¼±Č“潚ŹōøüŅ×±»øÆŹ“
D£®Ķ°åÉĻµÄĢśĆ¶¤“¦ŌŚ³±ŹŖµÄæÕĘųÖŠ·¢Éś£ŗFe£3e£===Fe3£«£¬“Ó¶ųŠĪ³ÉĢśŠā£¬µ«“Ė¹ż³ĢĶ²»±»øÆŹ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĶ¼±ķŹ¾µÄŹĒÄŃČÜĒāŃõ»ÆĪļŌŚ²»Ķ¬pHĻĀµÄČܽā¶Č£ØS£¬mol/L£©£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
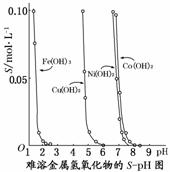
A£®pH£½3Ź±ČÜŅŗÖŠĢśŌŖĖŲµÄÖ÷ŅŖ“ęŌŚŠĪŹ½ŹĒFe3£«
B£®ČōNi£ØNO3£©2ČÜŅŗÖŠŗ¬ÓŠÉŁĮæµÄCo2£«ŌÓÖŹ£¬æÉĶعżµ÷½ŚČÜŅŗpHµÄ·½·ØĄ“³żČ„
C£®Čō·ÖĄėČÜŅŗÖŠµÄFe3£«ŗĶCu2£«£¬æɵ÷½ŚČÜŅŗµÄpHŌŚ4×óÓŅ
D£®ČōŌŚŗ¬ÓŠCu2£«ŗĶNi2£«µÄČÜŅŗÖŠ¼ÓČėÉÕ¼ī£¬Ni£ØOH£©2ÓÅĻČ³Įµķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ0.1mol•L﹣1“×ĖįČÜŅŗµÄpH=a£¬ĻĀĮŠÄÜŹ¹ČÜŅŗpH=£Øa+1£©µÄ“ėŹ©ŹĒ£Ø””””£©
| ”” | A£® | ½«ČÜŅŗĻ”ŹĶµ½ŌĢå»żµÄ10±¶ |
| ”” | B£® | ¼ÓČėŹŹĮæµÄ“×ĖįÄĘ¹ĢĢå |
| ”” | C£® | ¼ÓČėµČĢå»ż0.2 mol•L﹣1ŃĪĖį |
| ”” | D£® | ĢįøßČÜŅŗµÄĪĀ¶Č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŅŃÖŖ£ŗCH3CH2CH2CH3£Øg£©+6.5O2£Øg£©═4CO2£Øg£©+5H2O£Øl£©”÷H=﹣2878kJ•mol﹣1£¬£ØCH3£©2CHCH3£Øg£©+6.5O2£Øg£©═4CO2£Øg£©+5H2O£Øl£©”÷H=﹣2869kJ•mol﹣1ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | Õż¶”Ķé·Ö×Ó“¢“ęµÄÄÜĮæ“óÓŚŅģ¶”Ķé·Ö×Ó |
| ”” | B£® | Õż¶”ĶéµÄĪČ¶ØŠŌ“óÓŚŅģ¶”Ķé |
| ”” | C£® | Ņģ¶”Ķé×Ŗ»ÆĪŖÕż¶”ĶéµÄ¹ż³ĢŹĒŅ»øö·ÅČČ¹ż³Ģ |
| ”” | D£® | Ņģ¶”Ķé·Ö×ÓÖŠµÄĢ¼Ēā¼ü±ČÕż¶”ĶéµÄ¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚŗćĪĀĢõ¼žĻĀ£¬ÓŠ¼×”¢ŅŅĮ½ČŻĘ÷£¬¼×ČŻĘ÷ĪŖĢå»ż²»±äµÄĆܱÕČŻĘ÷£¬ŅŅČŻĘ÷ĪŖŅ»øö“ųÓŠĄķĻė»īČū£Ø¼“ĪŽÖŹĮ攢ĪŽÄ¦²ĮĮ¦µÄøÕŠŌ»īČū£©µÄĢå»żæɱäµÄĆܱÕČŻĘ÷£¬Į½ČŻĘ÷ĘšŹ¼×“Ģ¬ĶźČ«ĻąĶ¬£¬¶¼³äÓŠCĘųĢ壬Čō·¢ÉśæÉÄę·“Ó¦C£Øg£©⇌A£Øg£©+B£Øg£©£¬¾Ņ»¶ĪŹ±¼äŗ󣬼ה¢ŅŅĮ½ČŻĘ÷·“Ó¦¶¼“ļµ½Ę½ŗā£®ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | Ę½ŗāŹ±CµÄ×Ŗ»ÆĀŹ£ŗŅŅ£¾¼× | B£® | Ę½ŗāŹ±CµÄĢå»ż·ÖŹż£ŗŅŅ£¾¼× |
| ”” | C£® | ·“Ó¦ĖŁĀŹ£ŗŅŅ£¾¼× | D£® | Ę½ŗāŹ±AµÄĪļÖŹµÄĮæ£ŗ¼×£¾ŅŅ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ŌŚĆܱÕČŻĘ÷ÖŠ½ųŠŠČēĻĀ·“Ó¦£ŗX£Øg£©+Y£Øg£©⇌2Z£Øg£©£¬ŅŃÖŖX”¢Y”¢ZµÄĘšŹ¼ÅØ¶Č·Ö±šĪŖ0.1mol/L”¢0.2mol/L”¢0.2mol/L£¬ŌŚŅ»¶ØĢõ¼žĻĀ£¬“ļµ½Ę½ŗāŹ±£¬ø÷ĪļÖŹµÄÅØ¶Č²»æÉÄÜŹĒ£Ø””””£©
| ”” | A£® | ZĪŖ0.3 mol/L | B£® | YĪŖ0.15 mol/L |
| ”” | C£® | XĪŖ0.1 mol/L | D£® | ZĪŖ0.4 mol/L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÖųĆū»Æѧ¼ŅŠģ¹āĻÜ»ńµĆ¹ś¼Ņ×īøßæĘѧ¼¼Źõ½±£¬ŅŌ±ķÕĆĖūŌŚĻ”ĶĮŻĶČ”ĄķĀŪ·½Ćę×÷³öµÄ¹±Ļ×£®ŅŃÖŖ£ŗ½šŹōīę£ØĻ”ĶĮŌŖĖŲ£©ŌŚæÕĘųÖŠŅ×Ńõ»Æ±ä°µ£¬ŹÜČČŹ±Č¼ÉÕ£¬ÓöĖ®ŗÜæģ·“Ó¦£®£Ø×¢£ŗīę³£¼ūµÄ»ÆŗĻ¼ŪĪŖ+3ŗĶ+4£¬Ńõ»ÆŠŌ£ŗCe4+£¾Fe3+£¾I2£®£©ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø£©
A£® īęČÜÓŚĒāµāĖįµÄ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗCe+4HI  CeI4+2H2”ü
CeI4+2H2ӟ
B£® ÓĆCe£ØSO4£©2ČÜŅŗµĪ¶ØĮņĖįŃĒĢśČÜŅŗ£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ£ŗCe4++2Fe2+═Ce3++2Fe3+
C£® ½šŹōCe±£“ꏱ£¬Ó¦øĆøō¾ųæÕĘųŗĶĖ®
D£® īęµÄĖÄÖÖŗĖĖŲ13658Ce”¢13858Ce”¢14058Ce”¢14258Ce£¬ĖüĆĒ»„³ĘĪŖĶ¬ĖŲŅģŠĪĢå
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com