

分析 (1)一水合氨为弱碱,部分电离,存在电离平衡,依据影响电离平衡因素解答;
(2)依据所给的反应物和产物,结合元素守恒书写方程式即可,依据反应书写平衡常数表达式;
(3)电解NO制备NH4NO3,由图可知乙为阳极反应为NO-3e-+2H2O=NO3-+4H+,甲为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,据此解答.
解答 解:(1)一水合氨为弱碱,部分电离,存在电离平衡,电离方程式:NH3•H2O$\stackrel{.}{?}$NH4++OH-,往0.1mol•L-1的氨水中加入少量的NH4Cl固体,增大氨根离子浓度平衡左移,氢氧根离子浓度减小,溶液pH值降低;
明矾电离产生铝离子,铝离子与氢氧根离子反应,消耗氢氧根离子,促进一水合氨电离,铵根离子浓度增大;
故答案为:NH3•H2O$\stackrel{.}{?}$NH4++OH-;降低; 增大;
(2)硝酸铵分解生成N2O和H2O,达到平衡,说明为可逆反应,化学反应方程式为:NH4NO3$\stackrel{250℃}{?}$ N2O+2H2O,250℃时,水为气体状态,故平衡常数K=c(N2O)×c2(2H2O);
故答案为:NH4NO3$\stackrel{250℃}{?}$N2O+2H2O;K=c(N2O)c(H2O)2;
(3)电解NO制备NH4NO3,由图可知乙为阳极反应为NO-3e-+2H2O=NO3-+4H+,甲为阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O$\frac{\underline{\;通电\;}}{\;}$3NH4NO3+2HNO3,因此若要使电解产物全部转化为NH4NO3,需补充NH3,
故答案为:NH3;根据电子守恒,阳极得到的NO3-的量大于阴极得到的NH4+的量,所以需充入NH3;
点评 本题考查了元素化合物知识,熟悉氮及其化合物性质、弱电解质电离平衡影响因素、电解池工作原理是解题关键,题目难度中等.


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:选择题
| A. | 除③外 | B. | 除④外 | C. | 除③④外 | D. | 除②⑥外 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使酚酞变红色的溶液:Mg2+、K+、SO42-、NO3- | |
| B. | NaClO和NaCl混合溶液中:H+、NH4+、SO42-、Br- | |
| C. | 氯化亚铁溶液中:Na+、Ba2+、Br-、NO3- | |
| D. | 0.1 mol•L-1的NaAlO2 溶液:H+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若甲为AlCl3,则丁可能是NaOH | B. | 若甲为乙醇,则丙可能是乙酸 | ||
| C. | 若甲为Fe,则丁可能是稀硝酸 | D. | 若甲为NaOH 溶液,则丁可能是CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 2014年世界杯足球赛在巴西举行,2016年巴西又将举办31届奥运会.奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质,能满足如图中阴影部分关系的是( )
2014年世界杯足球赛在巴西举行,2016年巴西又将举办31届奥运会.奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质,能满足如图中阴影部分关系的是( )| ① | ② | ③ | ④ | |
| A | NaCl | K2SO4 | KCl | (NH4)2SO4 |
| B | Na2SO4 | K2SO4 | KCl | NH4Cl |
| C | NaCl | K2SO4 | KCl | NH4Cl |
| D | Na2SO4 | K2SO4 | KCl | (NH4)2SO4 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,CO2的结构式为O=C=O.
,CO2的结构式为O=C=O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀H2SO4 反应:Ba2++SO42-=BaSO4↓ | |
| D. | 氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
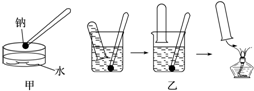 金属钠与水的反应是中学化学中的一个重要反应.该反应的演示方法分别如图甲、乙所示:
金属钠与水的反应是中学化学中的一个重要反应.该反应的演示方法分别如图甲、乙所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com