
下列常用实验室仪器中,一般不用于混合物分离或提纯的是
A.  B.
B.  C.
C.  D.
D. 
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列说法正确的是
A.铝箔在空气中受热熔化,并不滴落,说明铝与氧气没有发生化学反应
B.硅在电子工业中是最重要的半导体材料,广泛用于制作光导纤维
C.二氧化硫是一种有毒气体,所以不能用于杀菌消毒
D.氨很容易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求完成下面每一小题.
 (1).某烷烃的一个分子里含有9个碳原子,其一氯代物只有两种,该烷烃的系统名称是
(1).某烷烃的一个分子里含有9个碳原子,其一氯代物只有两种,该烷烃的系统名称是
(2)有机物A的结构简式为
①若A是单烯烃与氢气加成后的产物,则该单烯烃可能有____________种结构;
②若A是炔烃与氢气加成后的产物,则此炔烃可能有________种结构。
③若A的一种同分异构体只能由一种烯烃加氢得到,且该烯烃是一个非常对称的分子构型。写出A的该种同分异构体的结构简式:_______________________________________(写两种)
(3)一种由电石为原料合成的烃,其分子式为C4H4,它是合成一种橡胶的中间体,它有多种同分异构体。
请完成下列问题:
①它的一种链式结构,能使酸性高锰酸钾褪色,写出其结构简式是_____________。
②它的一种同分异构体,每个碳均达饱和,不能使酸性高锰酸钾褪色,且构成的空间构型中碳与碳间的夹角都相同,该结构式
查看答案和解析>>
科目:高中化学 来源: 题型:
同温同压下,两个等体积的干燥圆底烧瓶中分别充满①NH3,②NO2,进行喷泉实验,经充分反应后,瓶内溶液的物质的量浓度为( )
A.①>② B.①<② C.①=② D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
a、b、c、d、e是含有一种相同元素的五种物质,可发生如下转化:
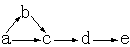 其中: a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应
其中: a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应
的水化物。已知H2S在足量氧气中燃烧生成SO2。
(1)如果a是一种淡黄色粉末固体,试推断这五种物质(用名称表示):
a ;b ;c ;d ;e 。
(2)如果a是一种常见气体,试推断这五种物质(用化学式表示):
a ;b ;c ;d ;e 。
查看答案和解析>>
科目:高中化学 来源: 题型:
反应 在一密闭容器中进行,则下列说法或结论中,能够成立的是
在一密闭容器中进行,则下列说法或结论中,能够成立的是
A.其他条件不变仅将容器的体积缩小一半,反应速率减小
B.反应达平衡状态时:v(CO)(正)=v(H2O)(逆)
C.保持体积不变,充入少量He使体系压强增大反应速率一定增大
D.其他条件不变,适当增加C(s)的质量会使反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——物质结构与性质】(15分)
三氟化氮是一种无色、无味、无毒且不可燃的气体,在半导体加工,太阳能电池制造和液晶显示器制造中得到广泛应用。NF3是一种三角锥型分子,键角102 °,沸点-129 ℃;可在铜的催化作用下由F2和过量NH3反应得到。

(1)写出制备 NF3的化学反应方程式: 。
(2)NF3的沸点比NH3的沸点(-33 ℃)低得多的主要原因是 。
(3)与铜属于同一周期,且未成对价电子数最多的元素基态原子核外电子排布式为 。
(4)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1 ),回答下面各题:
| 元素代号 | I1 | I2 | I3 | I4 |
| Q | 2080 | 4000 | 6100 | 9400 |
| R | 500 | 4600 | 6900 | 9500 |
| S | 740 | 1500 | 7700 | 10500 |
| T | 580 | 1800 | 2700 | 11600 |
| U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一族的是 和 。
②T元素最可能是 区元素。若T为第二周期元素,E是第三周期元素中原子半径最小的元素,则T、E形成化合物的空间构型为 ,其中心原子的杂化方式为 。
⑸与铜同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,产生的现象是 ;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 。
⑹在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中
金红石的晶胞如右图所示,则其中Ti4+的配位数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com