
在![]() (正反应为放热反应)的平衡体系,若想使
(正反应为放热反应)的平衡体系,若想使![]() 加快,平衡向正方向移动,提高
加快,平衡向正方向移动,提高![]() 转化率,应当采取的正确措施是
转化率,应当采取的正确措施是
[
]A
.增大氧气浓度 B.增大C
.增大压强 D.减小科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
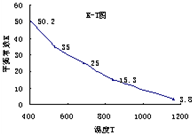 (2009?茂名二模)碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-.已知在不同温度下该反应的平衡常数如图,下列说法不正确的是( )
(2009?茂名二模)碘在水中溶解度很小,但易溶于KI溶液,因为发生反应:I2(aq)+I-(aq)=I3-.已知在不同温度下该反应的平衡常数如图,下列说法不正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
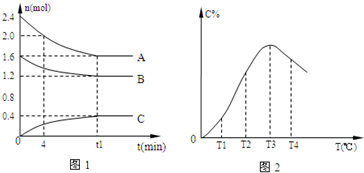
| A、0~4分钟时,A的平均反应速率为0.02mol/(L?min) | ||
B、该反应的平衡常数表达式K=
| ||
| C、由T1向T2变化时,V正>V逆 | ||
| D、此反应的正反应为放热反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com