
| A. | Fe+2FeCl3═3FeCl2 | B. | CH4+2O2=CO2+2H2O | ||
| C. | H2+Cl2=2HCl | D. | H2SO4+2NaOH═Na2SO4+2H2O |
分析 原电池反应必须是自发进行的放热的氧化还原反应,这几个条件必须同时具备才能设计成原电池,否则不能设计成原电池,据此分析解答.
解答 解:原电池反应必须是自发进行的放热的氧化还原反应,
A.该反应是自发进行的放热的氧化还原反应,所以能设计成原电池,故A不选;
B.该反应是自发进行的放热的氧化还原反应,所以能设计成原电池,故B不选;
C.该反应是自发进行的放热的氧化还原反应,所以能设计成原电池,故C不选;
D.该反应是复分解反应,没有电子转移,所以不能氧化还原反应,不能设计成原电池,故D选;
故选D.
点评 本题考查原电池设计,为高频考点,明确原电池原理是解本题关键,原电池反应必须具有“自发进行”、“放热”、“氧化还原反应”特点,题目难度不大.


科目:高中化学 来源: 题型:选择题
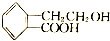 的有机物可以通过不同的反应得到下列五种物质
的有机物可以通过不同的反应得到下列五种物质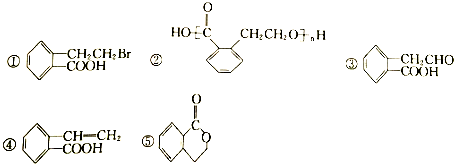
| A. | 取代、加成、氧化、消去、取代 | B. | 取代、取代、还原、消去、酯化 | ||
| C. | 酯化、缩聚、取代、消去、取代 | D. | 取代、缩聚、氧化、消去、酯化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水的摩尔质量为18g | |
| B. | 1 mol/L K2SO4溶液所含K+数目为2NA | |
| C. | 在常温常压下,2g氢气的体积为22.4L | |
| D. | 1 mol Mg2+的质量为24g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
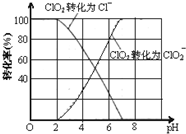 已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用.②ClO2气体在中性和碱性溶液中不能稳定存在.
已知:①ClO2气体只能保持在浓度较低状态下以防止爆炸性分解,且需现合成现用.②ClO2气体在中性和碱性溶液中不能稳定存在.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 放电时,电流从a极经负载后流向b极 | |
| B. | 充电时,Li+向a极移动 | |
| C. | 充电时a极发生的反应为:LiFePO4-xe-=Li1-xFePO4+xLi+ | |
| D. | 放电时,每转移xmol电子,产生1mol C6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Na2CO3溶液中CO32-的水解:CO32-+H2O═HCO3-+OH- | |
| C. | 用CuSO4溶液吸收H2S气体:Cu2++S2-═CuS↓ | |
| D. | 向NaOH溶液中通入过量的CO2气体:CO2+OH-═HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com