
分析 设出混合物中硫酸亚铁、硫酸铜及投入锌的物质的量,根据化学式可知,硫酸亚铁和硫酸铜的物质的量之和=硫酸根离子的物质的量,然后结合反应方程式及“剩余Fe2+的物质的量是溶液中Zn2+的物质的量的一半”列式计算出锌的物质的量,最后根据m=nM计算出其质量.
解答 解:剩余Fe2+的物质的量是溶液中Zn2+的物质的量的一半,说明亚铁离子部分被还原,则铜离子完全被还原成铜,
设FeSO4的物质的量为y mol,CuSO4的物质的量为x mol,投入的Zn为z mol,
根据反应Zn+CuSO4=Cu+ZnSO4可知反应后生成xmol锌离子,消耗了xmol锌,剩余锌的物质的量为:(z-x)mol,
根据反应Zn+FeSO4=Fe+ZnSO4可知,剩余Zn还原亚铁离子的物质的量为:(z-x)mol,剩余的亚铁离子的物质的量为:ymol-(z-x)mol=(x+y-z)mol,
剩余的2价铁离子的物质的量的是溶液中锌离子的物质的量的一半,则=(x+y-z)mol=0.5z,即:x+y=1.5Z,
30mLFeSO4和CuSO4的混合物(其中SO42-的物质的量浓度为0.1mol•L-1),则亚铁离子和铜离子的总物质的量=n(SO42-)=0.1mol/L×0.03L=0.003mol,
则:x+y=0.003mol=1.5z,
z=$\frac{0.003mol}{1.5}$=0.002mol,
所以加入锌的质量为:65g/mol×0.002mol=0.13g,
答:投入锌粉的质量为0.13g.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应原理为解答关键,注意掌握积累有关混合物反应的计算的方法与技巧,试题侧重考查学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题
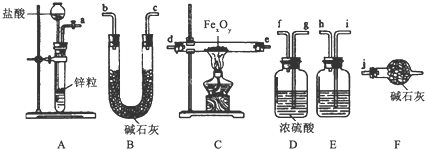
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 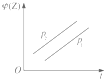 | B. | 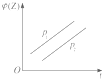 | C. | 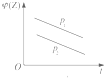 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{39ab}{4000-9a}$g | B. | $\frac{ab}{100}$g | C. | $\frac{39ab}{4000}$g | D. | $\frac{39ab}{4000+9a}$g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:1 | B. | 2:1:1 | C. | 2:1:2 | D. | 2:2:5 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg | B. | MgO | C. | Mg(OH)2 | D. | MgCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3,3-二甲基-4-乙基戊烷 | B. | 3,3,4-三甲基己烷 | ||
| C. | 1,3-二甲基-4-乙基己烷 | D. | 2,3-二乙基-4-甲基己烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com