
 如图,a曲线是198K、101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )
如图,a曲线是198K、101kPa时N2与H2反应过程中能量变化的曲线图,下列叙述正确的是( )科目:高中化学 来源:福建省古田一中2008-2009学年高二下学期半期考试化学试卷 题型:013
|
如图是198 K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是
| |
| [ ] | |
A. |
该反应的热化学方程式为: N2+3H2 |
B. |
a曲线是加入催化剂时的能量变化曲线 |
C. |
加入催化剂,该化学反应的反应热也改变 |
D. |
在温度体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ则184>Q2>2Q1 |
查看答案和解析>>
科目:高中化学 来源:新疆自治区月考题 题型:单选题
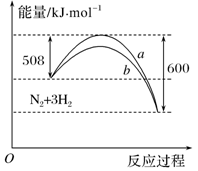
 2NH3 ΔH=-92 kJ/mol
2NH3 ΔH=-92 kJ/mol 查看答案和解析>>
科目:高中化学 来源:山西省模拟题 题型:单选题
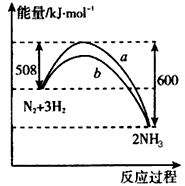
 2NH3 △H=-92 kJ/mol
2NH3 △H=-92 kJ/mol 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com