
| A. | 氯水中:2c(Cl2)=c(ClO-)+c(Cl-)+c(HClO) | |
| B. | 水的离子积常数Kw 随着温度的升高而增大,说明水的电离是放热反应 | |
| C. | 醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则b<a+1 | |
| D. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液:c(Na+)最小的是Na2CO3 |
分析 A.在氯水中存在三个平衡,使得氯水具有多样性:①Cl2+H2O?HCl+HClO ②HClO?H++ClO- ③H2O?H++OH-,氯元素守恒书写物料守恒判断;
B.水的电离过程为吸热过程;
C.醋酸为弱酸,加水稀释促进电离;
D.对应酸的酸性越弱,其盐的水解程度越大,溶液的碱性越强,溶液pH越大;当pH相同时,酸越强,盐的浓度越大.
解答 解:A.在氯水中存在三个平衡,使得氯水具有多样性:①Cl2+H2O?HCl+HClO ②HClO?H++ClO- ③H2O?H++OH-,氯元素守恒得到氯水中:c(Cl2)=2c(ClO-)+2c(Cl-)+2c(HClO),故A错误;
B.水的离子积常数Kw 随着温度的升高而增大,说明氢离子和氢氧根离子浓度增大,说明水的电离是吸热反应,故B错误;
C.醋酸为弱酸,加水稀释促进电离,应为b<a+1,故C正确;
D.pH相等的CH3COONa、NaOH和Na2CO3三种溶液,已知酸性:CH3COOH>H2CO3,所以水解程度:Na2CO3>CH3COONa,pH相同时,溶液的浓度:Na2CO3<CH3COONa,NaOH是强碱.c(Na+)最小,故D错误.
故选C.
点评 本题考查了电解质溶液中离子浓度大小、水的电离及其影响因素,盐类水解原理等知识点,掌握基础是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | s、p、d、f各能级的轨道数目分别为1、3、5、7 | |
| B. | 各电子层的能级都是从s能级开始至 f 能级结束 | |
| C. | 各电子层含有的能级数为(n-1) | |
| D. | 各电子层含有的电子数为2n2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
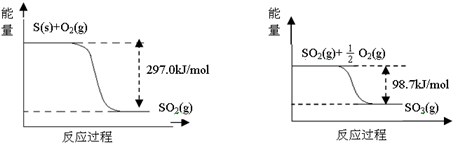
| A. | 1molS(g)与O2(g)完全反应生成SO2(g),反应放出的热量<297.0kJ | |
| B. | 在相同条件下,SO3(g)比SO2(g)稳定 | |
| C. | 1molSO2(g)和$\frac{1}{2}$molO2(g)生成1molSO3(g)放出98.7kJ的热量 | |
| D. | 由图得S(s)+$\frac{3}{2}$O2(g)?SO3(g)△H=-198.3kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属原子最外层电子的个数 | |
| B. | 1 mol金属与酸反应放出氢气的多少 | |
| C. | 1 mol金属失去电子的多少 | |
| D. | 金属原子失去电子的难易程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10Be和9Be是中子数不同质子数相同的不同原子 | |
| B. | 10Be的原子核内中子数比质子数多 | |
| C. | 2.6g26Al3+中所含的电子数约为6.02×1023 | |
| D. | 26Al3+和26Mg2+的质子数、中子数和电子数均不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用“84消毒液”进行消毒 | |
| B. | 用浓硫酸干燥二氧化硫气体 | |
| C. | 用活性炭吸附新装修居室里的有害气体 | |
| D. | 用小苏打治疗胃酸过多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com