
����Ŀ���������м����л��
A��![]() B��
B��![]() C��
C��![]() D��CH2 = CH��CH = CH2E��������
D��CH2 = CH��CH = CH2E��������
��1�������л����л�Ϊͬϵ�����_____________����Ϊͬ���칹�����____________��
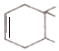
��2����ϵͳ��������B��������____________________________________��
��3��A��Cl2��Ӧ������Ϊ_____________��Dʹ��ˮ��ɫ�ķ�Ӧ����Ϊ___________��
��4��B�����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ ____________________________________��
��5����ͼ��ʾ����һ�ֽ���˫ϩ�ϳɵ��л���Ӧ����д��B��D����˫ϩ�ϳ����ò���Ľṹ��ʽ__________________��
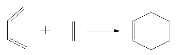
���𰸡� AC BE ![]() ��
��![]() ��ϩ ȡ����Ӧ �ӳɷ�Ӧ
��ϩ ȡ����Ӧ �ӳɷ�Ӧ 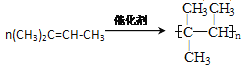
��������![]() ��
��![]() ������������Ϊͬϵ����
������������Ϊͬϵ����![]() ����ϩ����CH2 = CH��CH = CH2�Ƕ�ϩ����B��E�ķ���ʽ��ͬ����Ϊͬ���칹�壻��������ϩ��������ͬ��ͨʽ�����������̼ԭ������ͬʱ��Ϊͬ���칹�塣��������ȡ����Ӧ��ϩ�������ӳɷ�Ӧ�ͼӾ۷�Ӧ��
����ϩ����CH2 = CH��CH = CH2�Ƕ�ϩ����B��E�ķ���ʽ��ͬ����Ϊͬ���칹�壻��������ϩ��������ͬ��ͨʽ�����������̼ԭ������ͬʱ��Ϊͬ���칹�塣��������ȡ����Ӧ��ϩ�������ӳɷ�Ӧ�ͼӾ۷�Ӧ��
��1�������л����л�Ϊͬϵ�����AC����Ϊͬ���칹�����BE��
��2����ϵͳ��������B��������Ϊ![]() ��
��![]() ��ϩ��
��ϩ��
��3��A��Cl2�ڹ��յ������¿��Է���ȡ����Ӧ��D��������2��̼̼˫��������ʹ��ˮ��ɫ�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��
��4��B�����Ӿ۷�Ӧ�Ļ�ѧ����ʽΪ ��
��
��5����˫ϩ�ϳɵ��л���Ӧ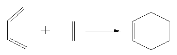 ��֪��B��D����˫ϩ�ϳ����ò���Ľṹ��ʽΪ
��֪��B��D����˫ϩ�ϳ����ò���Ľṹ��ʽΪ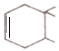 ��
��


 ����ʦ��Сһ����ʦ������ҵϵ�д�
����ʦ��Сһ����ʦ������ҵϵ�д� ���100�ֵ�Ԫ�Ż�������ϵ�д�
���100�ֵ�Ԫ�Ż�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£������������ǿ��淴ӦA(g)+3B(g)2C(g)�ﵽƽ���־����( )
��C������������C�ķֽ�������ȣ�
�ڵ�λʱ������amol A��ͬʱ����3amolB��
��A��B��C��Ũ�Ȳ��ٱ仯��
��A��B��C�����ʵ������ٱ仯
A.��B.��C.��D.��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����( )
A.���ԣ�LiOH��NaOH��KOH��RbOHB.�����ԣ�Li��Na��K��Rb
C.ԭ�Ӱ뾶��Li��Na��K��RbD.�۷е㣺Li��Na��K��Rb
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪HClO�����Ա�H2CO3�������з�ӦCl2+H2OHCl+HClO�ﵽƽ���Ҫʹƽ����ϵ��HClO��Ũ������Ӧ��ȡ�ķ����ǣ�������
A.����ʯ��ʯ
B.����
C.�������NaOH
D.��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���pH=11��ij��Һ�У���ˮ�����c��OH����Ϊ��������
��1.0��10��7 molL��1����1.0��10��6 molL��1
��1.0��10��3 molL��1����1.0��10��11 molL��1 ��
A.��
B.��
C.�ٻ��
D.�ۻ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ3Fe��s��+4H2O��g�� ![]() Fe3O4��s��+4H2��g����һ�ɱ��ݻ����ܱ������н��У��Իش�
Fe3O4��s��+4H2��g����һ�ɱ��ݻ����ܱ������н��У��Իش�
��1������Fe�������䷴Ӧ����������������䡱��С������ͬ����
��2���������������Сһ�룬�䷴Ӧ���� ��
��3������������䣬����N2ʹ��ϵѹǿ�����䷴Ӧ���� ��
��4������ѹǿ���䣬����N2ʹ��������������䷴Ӧ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ����٤��������ֵ������������ȷ���ǣ�������
A.���³�ѹ�£�22.4LCO2���еķ�����Ϊ1NA
B.���³�ѹ�£�1.06gNa2CO3���е�Na+������Ϊ0.02NA
C.ͨ��״���£�NA��CO2����ռ�е����ԼΪ22.4L
D.���ʵ���Ũ��Ϊ0.5mol/L��MgCl2��Һ�У�����Cl������Ϊ1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ���ǣ�������
A.�����������ȷ�Ӧұ�����۵�Ľ���
B.�ִ�ʯ�ͻ���������������������ʵ��һ�������ϩת��Ϊ��������Ĺ��̣��÷�Ӧ��ԭ��������Ϊ100%
C.��ҵ�����������ữ��Ũ����ˮ��ֱ��ͨ�������û����弴��
D.úֱ��Һ���ɵ�Һ��ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩ��һ����Ҫ�Ļ���ԭ�ϣ���������Ϊԭ����ȡ���ش��������⡣
��1����ͳ�����ѽⷨ���ִ��������ѽⷨ���Ȼ�ѧ����ʽ���£�
��C2H6(g)=C2H4(g) +H2(g) ��H1=+136 kJ/mol
��C2H6(g)+ ![]() O2(g)= C2H4(g)+H2O(g) ��H2=-110 kJ/mol
O2(g)= C2H4(g)+H2O(g) ��H2=-110 kJ/mol
��֪��Ӧ��صIJ��ֻ�ѧ�������������£�
��ѧ�� | H-H(g) | H-O(g) | O=O(g) |
����( kJ/mol) | 436 | X | 496 |
�ɴ˼���x=_________��ͨ���Ƚϡ�H1�͡�H2��˵�������ѽⷨ��ȣ������ѽⷨ���ŵ���_______________________________����дһ�㣩��
��2������������ѽⷴӦ�����г���C2H4�⣬������CH4��CO��CO2�ȸ��������Ӧ��Ϊ���ȷ�Ӧ����ͼ1Ϊ�¶ȶ����������ѽⷴӦ���ܵ�Ӱ�졣�����ת�������¶ȵ����߶����ߵ�ԭ����______����Ӧ������¶�Ϊ____________����ѡ����ţ���
A.700�� B.750�� C.850�� D.900��
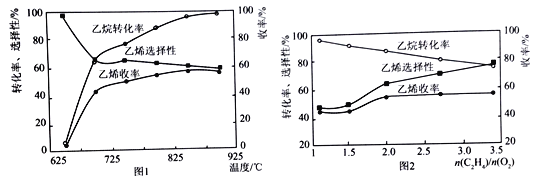
[��ϩѡ����=![]() ����ϩ����=����ת���ʡ���ϩѡ����]
����ϩ����=����ת���ʡ���ϩѡ����]
��3������������Ӧ�У����������ͻᵼ�·�Ӧ������̿��������Ӧ�ܡ�ͼ2Ϊn(C2H6)/n(O2)��ֵ�����������ѽⷴӦ���ܵ�Ӱ�졣�ж����������ѽ������n(C2H6)/n(O2)�����ֵ��_______________���жϵ�������__________________________________��
��4����ҵ�ϣ�������ϵ��ѹ�㶨Ϊ100kPa�������½��и÷�Ӧ��ͨ��������������Ļ�������в���������壨����������������Ϊ70%����������������Ŀ����___________________________��
��Ӧ��ƽ��ʱ������ֵ�����������±���
C2H6 | O2 | C2H4 | H2O | �������� |
2.4% | 1.0% | 12% | 15% | 69.6% |
������¶��µ�ƽ�ⳣ��Kp=_________����ƽ���ѹ����ƽ��Ũ�ȣ�ƽ���ѹ=��ѹ�����������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com