
下图所示的电解池Ⅰ和Ⅱ中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是( )

选项 | X | Y |
A. | MgSO4 | CuSO4 |
B. | AgNO3 | Pb(NO3)2 |
C. | FeSO4 | Al2 (SO4)3 |
D. | CuSO4 | AgNO3 |
D
【解析】
试题分析:装置图分析电极名称,a为阳极,b为阴极,c为阳极,d为阴极,结合电解原理,溶液中离子放电顺序分析判断电极反应,电极b和d上没有气体逸出,但质量均增大,说明阴极上溶液中金属离子在阴极析出金属单质。 A、X为MgSO4,阴极电极反应为溶液中氢离子放电,无金属析出;Y为CuSO4 ,溶液中阴极上铜离子得到电子析出金属,故A错误;B、X为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,Y为Pb(NO3)2 ,阴极上溶液中氢离子放电,无金属析出,故B错误;C、X为FeSO4,阴极是溶液中氢离子得到电子生成氢气,无金属析出,Y为Al2 (SO4)3,阴极上是氢离子放电无金属析出,故C错误;D、X为CuSO4,阴极是溶液中铜离子析出,电极反应Cu2++2e-=Cu,Y为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,依据电子守恒Cu~2Ag,增重d>b,符合题意,故D正确。
考点:本题考查电解原理及应用。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015届山东省泰安市高三上学期期中考试化学试卷(解析版) 题型:填空题
(8分)已知溶液中:还原性HSO3->I-,氧化性IO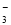 >I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
>I2>SO42-。向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示。
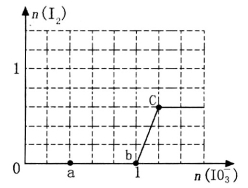
试回答下列问题:
(1)写出a点反应的离子方程式____________;反应中还原剂是_______;被还原的元素是________。
(2)写出b点到c点反应的离子方程式_______________。
(3)若往100mL 1 mol·L-1的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第一次(10月)检测化学试卷(解析版) 题型:选择题
下列关于实验操作的说法正确的是 ( )
A.可用25 mL碱式滴定管量取20.00 mL KMnO4溶液
B.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干
D.将金属钠在研钵中研成粉末,使钠与水反应的实验更安全
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三上学期第二次检测化学试试卷(解析版) 题型:选择题
下列实验装置、选用的试剂或实验操作中,都正确的是
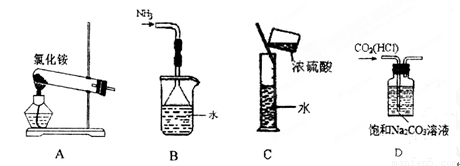
A.实验室用装置A制取氨气 B.用B装置吸收氨气,并防止倒吸
C.用C装置稀释浓硫酸 D.用D装置除去CO2中的HCl
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:填空题
(12分)运用化学反应原理研究元素及其化合物的反应有重要意义。
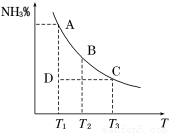
工业合成氨过程中,N2和H2反应生成NH3:N2(g)+3H2(g) 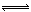 2NH3(g)。混合体系中NH3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
2NH3(g)。混合体系中NH3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态)。根据图示回答下列问题:
(1)N2(g)+3H2(g) 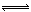 2NH3(g)的ΔH________0(填“>”或“<”)。
2NH3(g)的ΔH________0(填“>”或“<”)。
(2)若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡_______移动(填“向左”、“向右”或“不移动”) 。
(3)若温度为T1时,反应进行到状态D时,v正_____v逆(填“>”、“<”或“=”)。
(4)在体积为5 L的恒温、恒容密闭容器中,起始时投入2 mol N2、3 mol H2,经过10 s达到平衡,测得平衡时NH3的物质的量为0.8 mol。
①达平衡时N2的转化率=________。
②容器中反应的逆反应速率随时间变化的关系如图。
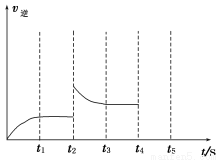
t2时改变了某一种条件,改变的条件可能是__________、____________________(填写两项)。
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:选择题
臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)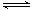 N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是( )
A | B |
|
|
升高温度,NO2的含量减小 | 0~3 s内,反应速率为 v(NO2)=0.2 mol·L-1 |
C | D |
|
|
t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x可能为压强 |
查看答案和解析>>
科目:高中化学 来源:2015届山东省高三第一次学情调查化学试卷(解析版) 题型:选择题
反应:L(s)+aG(g) bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。
bR(g) 达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数。
据此可判断

A.上述反应是放热反应 B.上述反应是吸热反应
C.a>b D.无法判断a,b大小
查看答案和解析>>
科目:高中化学 来源:2015届山东省文登市高三上学期11月月考化学试卷(A卷)(解析版) 题型:选择题
根据表中信息,判断下列叙述中正确的是
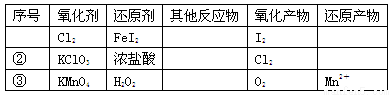
A.表中①组的反应中氧化产物一定是I2
B.氧化性强弱的比较:KClO3>Cl2>Fe3+>I2
C.表中②组每生成1molCl2,转移1mol电子
D.表中③组其他反应物可以为浓盐酸
查看答案和解析>>
科目:高中化学 来源:2015届山东省德州市高三10月月考化学试卷(解析版) 题型:选择题
下列是某同学对相应的离子方程式所作的评价,其中评价合理的是
编号 | 化学反应 | 离子方程式 | 评 价 |
A | 碳酸钙与醋酸反应 | CO32-+2CH3COOH =CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解质,不应写成离子形式 |
B | NaAlO2溶液中通入过量CO2 | 2AlO2-+CO2+3H2O==2Al(OH)3↓+CO32- | 正确 |
C | NaHCO3的水解 | HCO3-+H2O ═ CO32-+H3O+ | 错误,水解方程式误写成电离方程式 |
D | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com