
| 实验编号 | 反应物 | 催化剂 |
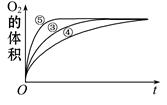
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol·L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol·L-1FeCl3溶液 |



科目:高中化学 来源:不详 题型:单选题
| 选项 | 反应 温度 | 反 应 物 | H2O | |||
| Na2S2O3 | H2SO4 | |||||
| t(℃) | V(mL) | c(mol×L-1) | V(mL) | c(mol×L-1) | V(mL) | |
| A | 10 | 5 | 0.1 | 10 | 0.1 | 10 |
| B | 10 | 5 | 0.1 | 5 | 0.1 | 30 |
| C | 30 | 5 | 0.1 | 5 | 0.1 | 10 |
| D | 30 | 5 | 0.2 | 5 | 0.2 | 35 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.温度越低,化学反应越慢 | B.低温下分子无法运动 |
| C.温度降低,化学反应停止 | D.化学反应前后质量守恒 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 实验 | 反应温度/℃[ | Na2S2O3溶液 | 稀H2SO4 | ||
| V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 |
| B | 25 | 5 | 0.2 | 5 | 0.2 |
| C | 35 | 5 | 0.1 | 10 | 0.1 |
| D | 35 | 5 | 0.2 | 5 | 0.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入NH4HSO4固体,v(H2)不变 |
| B.加入少量水,v(H2)减小 |
| C.加入CH3COONa固体,v(H2) 不变 |
| D.滴加少量CuSO4溶液,v(H2)减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 实验 序号 | 初始浓度c/mol·l-1 | 溴颜色消失 所需时间t/s | ||
| CH3CO CH3 | HCl | Br2 | ||
| ① ② ③ ④ | 0.80 1.60 0.80 0.80 | 0.20 0.20 0.40 0.20 | 0.0010 0.0010 0.0010 0.0020 | 290 145 145 580 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2O4,测得NO2转化率为a%,在温度、体积不变时,再通入1mol NO2,待重新建立平衡时,测得NO2转化率为b%,a与b比较( )
N2O4,测得NO2转化率为a%,在温度、体积不变时,再通入1mol NO2,待重新建立平衡时,测得NO2转化率为b%,a与b比较( )| A.a>b | B.a<b | C.a="b" | D.无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com