
| A. | 主族序数等于原子最外层电子数 | |
| B. | 主族元素最高正化合价等于最外层电子数 | |
| C. | 第n主族元素其最高正化合价为+n价,最低负化合价绝对值为8-n(n≥4) | |
| D. | 第n主族元素其最高价氧化物分子式为R2On,氢化物分子式为RHn(n≥4) |
分析 对于主族元素,电子层数=周期数,最外层电子数=族序数;最高正价=最外层电子数,非金属元素最高正价+最低负价绝对值=8(H元素除外).
解答 解:A、对于主族元素,电子层数=周期数,最外层电子数=族序数,故A正确;
B、对于主族元素,最高正价=最外层电子数(氧元素、氟元素一般没有正化合价),故B正确;
C、对于主族元素,非金属元素最高正价+最低负价绝对值=8(H元素除外),故C正确;
D、第n主族元素其最高价氧化物对应的化学式为R2On,最高正化合价为+n,所以最低负价为-(8-n),所以氢化物化学式为RH(8-n)(n≥4)或H(8-n)R,故D错误.
故选:D.
点评 考查原子结构、性质、位置关系,难度较小,注意D项主族元素最高正价+最低负价绝对值=8.


科目:高中化学 来源: 题型:选择题
| A. | C4H8O3的结构简式为HOCH2CH2CH2COOH | |
| B. | C4H8O3的结构简式为CH3CH(OH)CH2COOH | |
| C. | C4H8O3为α-羟基丁酸 | |
| D. | C4H8O3为羟基乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
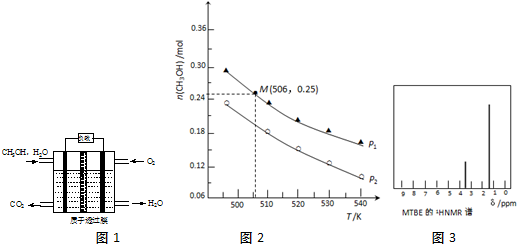
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若生成NA个水蒸气分子反应热为△H0,则△H0<△H | |
| B. | 当有20NA个电子转移时,放出2600kJ 热量 | |
| C. | 当有4NA个碳氧共用电子对生成时,放出1300kJ热量 | |
| D. | 上述反应为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
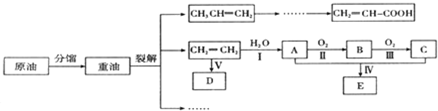
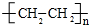 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | H+ | Na+ | NH4+ | NO3- | SO42- |
| 浓度(mol/L) | 1×10-5 | 2×10-5 | 3×10-5 | 4×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 操 作 | 现 象 |
通入氯气至过量 | I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com