
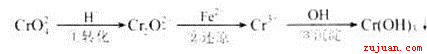
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O Cr3+ (aq)+3OH—(aq)
Cr3+ (aq)+3OH—(aq)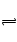 Cr2O72-(橙色)+H2O,平衡右移,呈橙色(2)能说明第①步反应达平衡状态的是溶液的颜色不变,溶液的各反应混合物浓度不变,选c(3)由得失电子守恒得:1mol Cr2O72―变6价,要6molFe2+ (4)Ksp=c(Cr3+)·c3(OH-)=10-32,c3(OH-)= 10-32/10-5=10-27,c(OH-)= 10-9mol·L-1,pH= 5(5)阳极反应为Fe-2e-=Fe2+,提供还原剂Fe2+;所以用铁作电极(6)在阴极附近溶液pH升高的原因是2H++2e-=H2↑,水电离平衡被破坏,留下OH―,提高碱度,使Cr(OH)3、Fe(OH)3沉淀而除去。
Cr2O72-(橙色)+H2O,平衡右移,呈橙色(2)能说明第①步反应达平衡状态的是溶液的颜色不变,溶液的各反应混合物浓度不变,选c(3)由得失电子守恒得:1mol Cr2O72―变6价,要6molFe2+ (4)Ksp=c(Cr3+)·c3(OH-)=10-32,c3(OH-)= 10-32/10-5=10-27,c(OH-)= 10-9mol·L-1,pH= 5(5)阳极反应为Fe-2e-=Fe2+,提供还原剂Fe2+;所以用铁作电极(6)在阴极附近溶液pH升高的原因是2H++2e-=H2↑,水电离平衡被破坏,留下OH―,提高碱度,使Cr(OH)3、Fe(OH)3沉淀而除去。

科目:高中化学 来源:不详 题型:单选题
 H2(g)+I2(g)达到平衡后,下列说法中,正确的是:
H2(g)+I2(g)达到平衡后,下列说法中,正确的是:
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
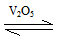 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是| A.催化剂V2O5增加该反应的正反应速率而不改变逆反应速率 |
| B.增大反应体系的压强,反应速率一定增大 |
| C.进入接触室的SO2和空气必须进行净化,且该反应不需要在高压下进行 |
| D.该反应是放热反应,降低温度将缩短反应达到平衡的时间 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g);△H<0。该反应的速率与时间的关系如下图所示:
2C(g);△H<0。该反应的速率与时间的关系如下图所示: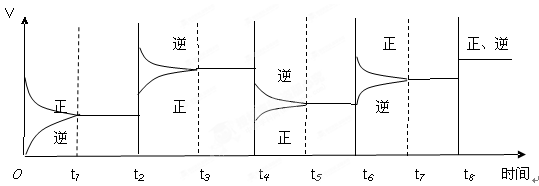
| A.降低温度、增大压强、减小反应物浓度、使用了催化剂 |
| B.使用了催化剂、增大压强、增大反应物浓度、升高温度 |
| C.增大反应物浓度、使用了催化剂、减小压强、升高温度 |
| D.升高温度、减小压强、增大反应物浓度、使用了催化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 p C(g) + q D(g)的反应中,(m.n.p. q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为
p C(g) + q D(g)的反应中,(m.n.p. q为各物质的化学计量数),经5min达到平衡,测得:A增加3 mol·L-1,B增加1 mol·L-1,C减少2 mol·L-1,此时若给体系加压,平衡不移动,则m :n :p :q为| A.2 :3 :2 : 3 | B.2 :2 :3 : 3 |
| C.3 :1 :2 : 2 | D.3 :1 :2 : 3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 4NO2(g)+ O2(g);△H >0,T1温度下的部分实验数据如下表.下列说法不正确的是
4NO2(g)+ O2(g);△H >0,T1温度下的部分实验数据如下表.下列说法不正确的是 | t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 B + C在某一温度时,达到平衡。
B + C在某一温度时,达到平衡。 向逆反应方向移动,则A呈___________态;
向逆反应方向移动,则A呈___________态; 正向、逆向、不)
正向、逆向、不)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g) 并达到平衡,甲容器保持体积不变, C的体积分数为m%;乙容器保持压强不变,C的体积分数为n%,则m和n的正确关系为
2C(g) 并达到平衡,甲容器保持体积不变, C的体积分数为m%;乙容器保持压强不变,C的体积分数为n%,则m和n的正确关系为 | A.m<n | B.m="n" | C.m>n | D.无法比较 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com