
| A. | 通式相同的不同物质一定属于同系物 | |
| B. | 完全燃烧某有机物,生成CO2和H2O的物质的量之比为1:1,该有机物只可能是烯烃或环烷烃 | |
| C. | 分子式相同而结构不同的化合物一定互为同分异构体 | |
| D. | 符合通式CnH2n-2的有机物一定是炔烃 |
分析 A.互为同系物的有机物必须具有相似结构,通式相同的有机物不一定具有相似结构,如烯烃与环烷烃的通式相同,它们的结构不同;
B.某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,说明有机物分子中C、H原子数目之比为1:2,该有机物可能为烃,也可能为烃的含氧衍生物;
C.同分异构体是分子式相同结构式不同的化合物;
D.二烯烃的通式符合符合通式CnH2n-2(n≥3).
解答 解:A.同系物之间具有相似结构,具有相同的通式,但是具有相同通式的有机物不一定互为同系物,如烯烃和环烷烃的通式相同,但是它们的结构不同,不属于同系物,故A错误;
B.某有机物在氧气里充分燃烧,生成的CO2和H2O的物质的量之比为1:1,说明有机物分子中C、H原子数目之比为1:2,该有机物可能为烃,也可能为烃的含氧衍生物,不能确定是否含有元素,故B错误;
C.分子式相同而结构不同的化合物互为同分异构体,故C正确;
D.符合通式CnH2n-2(n≥3)的有机物可能是二烯烃,故D错误;
故选C.
点评 本题考查同分异构体有关知识,为高频考点,明确同分异构体、同系物、同素异形体等基本概念内涵是解本题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:推断题
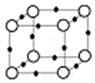 在周期表中1~36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子.Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
在周期表中1~36号之间的W、X、Y、Z、Q六种元素,它们的原子序数依次增大,已知W与其余五种元素既不同周期也不同主族,X原子的L层p轨道中有2个电子,Y元素原子的最外层有3个自旋方向相同的未成对电子,Z元素原子基态时,核外电子排布在3个能级上,且有2个未成对电子.Q元素在第四周期,原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 依据分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等 | |
| B. | 依据是否有电子转移,将化学反应分为氧化还原反应和非氧化还原反应 | |
| C. | 依据分散质粒子直径的大小,将分散系分为溶液、胶体、浊液 | |
| D. | 依据组成元素的种类,将纯净物分为单质和化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH═Na++O2-+H+ | B. | MgCl2═Mg2++Cl22- | ||
| C. | KClO3═K++Cl-+3O2- | D. | NH4NO3═NH4++NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
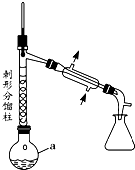 乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下:
乙酰苯胺具有解热镇痛作用,是较早使用的解热镇痛药,有“退热冰”之称,其制备原理如下: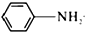 +CH3COOH$\stackrel{△}{?}$
+CH3COOH$\stackrel{△}{?}$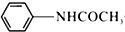 +H2O
+H2O| 物质 | 熔点 | 沸点 | 溶解度 |
| 乙酰苯胺 | 114.3℃ | 305℃ | 微溶于冷水、易溶于热水 |
| 苯胺 | -6℃ | 184.4℃ | 微溶于水 |
| 醋酸 | 16.6℃ | 118℃ | 易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
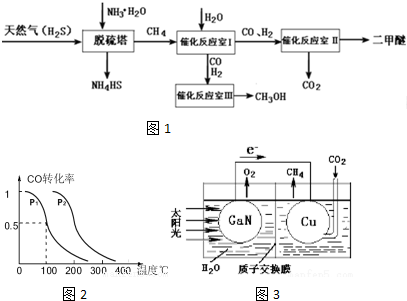
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com