
【题目】金属钛被用于航空航天工业、化工、医疗等领域。用钛铁矿(主要成份为FeTiO3)制取钛并获得副产品绿矾的工艺流程如下:
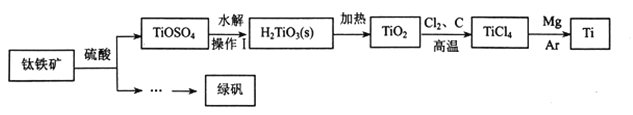
(1)TiOSO4中钛的化合价为_________,操作I的名称是为_________。
(2)TiOSO4经水解得H2TiO3的化学方程式为_________。
(3)TIO2与焦炭和Cl2在高温下反应得TiCl4井产生还原性气体,相应的化学方程式为_________。
(4)加热Mg与TiCl4得到钛时,Ar的作用是_________。
(5)某厂用3.8吨纯度为40%的钛铁矿制取钛,理论上至少需要氯气______L(标准状况下)。
(6)已知K3[Fe(CN)6](铁氰化钾》和K4[Fe(CN)6](亚铁氰化钾)能发生如下反应:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓(蓝色沉淀),4Fe3++3(Fe(CN)6]4-=Fe4[Fe(CN)6]3↓(蓝色沉淀)
①确定绿矾部分被氧化的方法是___________________________。(可供选择的试剂:铁氰化钾溶液、亚铁氧化钾溶液。铁粉、KSCN溶液)
②室温下,将绿矾配成0.1mol·L-1FeSO4溶液,测得溶液的pH=3,请用离子方程式解释原因_____________________,该溶液中c(SO42-)-c(Fe2+)≈_________________ mol·L-1。
【答案】 +4 过滤 TiOSO4+2H2O=H2TiO3↓+H2SO4 TiO2+2Cl2+2C![]() TiCl4+2CO 作保护气 4.48×105 取少许绿矾溶于水分装于两支试管中,分别滴加几滴铁氰化钾溶液、亚铁氰化钾溶液,若均有蓝色沉淀生成,则绿矾部分被氧化(合理即可) Fe2++2H2O=Fe(OH)2+2H+ 5×10-4
TiCl4+2CO 作保护气 4.48×105 取少许绿矾溶于水分装于两支试管中,分别滴加几滴铁氰化钾溶液、亚铁氰化钾溶液,若均有蓝色沉淀生成,则绿矾部分被氧化(合理即可) Fe2++2H2O=Fe(OH)2+2H+ 5×10-4
【解析】(1)TiOSO4中SO4为-2价,O为-2价,故Ti为+4价;TiOSO4经过水解生成H2TiO3固体沉淀,所以I操作为过滤;
(2)TiOSO4+2H2O=H2TiO3↓+H2SO4,此水解反应生成大量H2TiO3固体,且比较容易进行,所以要写沉淀符号,以及使用等号;
(3)还原性气体为CO,所以方程式为:TiO2+2Cl2+2C![]() TiCl4+2CO;
TiCl4+2CO;
(4)由于Mg是极为活泼的金属,需要隔绝空气进行反应,而惰性气体Ar的作用是作为保护气体;
(5)原材料中FeTiO3的物质的量为10000mol,每molTi需要与2molCl2结合,则共需要20000mol Cl2,标准状况下体积为4.48×105L。
(6)①绿矾部分被氧化,溶液中同时存在Fe2+和Fe3+离子,则应取少量绿矾溶液,先加入几滴铁氰化钾溶液、再加入几滴亚铁氰化钾溶液,若均有蓝色沉淀生成,则绿矾部分被氧化。
②FeSO4水解会生成Fe(OH)2从而消耗水电解生成的OH-,使溶液中H离子浓度增加,溶液呈酸性,离子方程式为:Fe2++2H2O=Fe(OH)2+2H+,Fe(OH)2为胶体不写沉淀符号。溶液的pH=3则c(H+)=1×10-3mol/L,相应降低溶液中消耗
c(Fe2+)= 0.5c(H+)=c(SO42-)-c(Fe2+)≈5×10-4mol·L-1。


科目:高中化学 来源: 题型:
【题目】下列有关电解质的叙述正确的是( )
A. 液态HCl不导电,所以HCl是非电解质
B. NH3的水溶液能够导电,所以NH3是电解质
C. 液态Cl2不导电,所以Cl2是非电解质
D. 熔融NaCl可以导电,所以NaCl是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列物质转化中,A是一种酸式盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:A![]() B
B![]() C
C![]() D
D![]() E。当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
E。当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是________,Z是________。
(2)当X是强酸时,写出B生成C的化学方程式________。
(3)当X是强碱时,E是________,写出E和铜反应生成C的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】断肠草(Gelsemium)为中国古代九大毒药之一,据记载能“见血封喉”,现代查明它是葫蔓藤科植物葫蔓藤,其中的毒素很多,下列是分离出来的四种毒素的结构式,下列推断正确的是

A. ①、②、③、④互为同分异构体
B. ①、③互为同系物
C. 等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者少
D. ①、②、③、④均能与氢氧化钠溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用密度为1.18 g·mL-1,质量分数为36.5%浓盐酸配制250 mL 0.1 mol·L-1 的盐酸,填空并回答下列问题:
(1)配制250 mL 0.1 mol·L-1的盐酸___________。
应称量盐酸体积/mL | 应选用容量瓶的规格/mL | 容量瓶外还需的其他仪器 |
(2)配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)___________。
A.用30 mL水洗涤烧杯和玻璃棒2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250 mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
(3)操作A中,将洗涤液都移入容量瓶,其目的是___________,溶液注入容量瓶前需恢复到室温,这是因为___________;
(4)若实验过程中出现如下情况如何处理?加蒸馏水时不慎超过了刻度线___________;向容量瓶中转移溶液时(实验步骤②)不慎有液滴掉在容量瓶外面___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度和压强下,将装有N2和NO2混合气体的试管倒立在水中,经足够的时间后,试管内气体的体积缩小为原体积的3/5,则原混合气体中N2和NO2体积比是
A. 2/3 B. 3/2 C. 3/5 D. 5/3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A. 30 g乙烷中所含的极性共价键数为7NA
B. 标准状况下,22.4 L N2和CO2混合气体所含的分子数为2NA
C. 1 L浓度为1 mol·L-1的 H2O2水溶液中含有的氧原子数为2NA
D. MnO2和浓盐酸反应生成1 mol氯气时,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g) + I2(g)![]() 2HI(g) ΔH=-a kJ·mol-1
2HI(g) ΔH=-a kJ·mol-1
已知: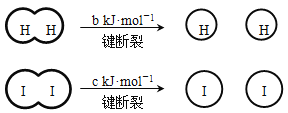 (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是( )
A. 反应物的总能量高于生成物的总能量
B. 断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量
C. 断开2 mol H-I键所需能量约为(c+b+a) kJ
D. 向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com